题目内容
17.下列离子方程式中正确的是( )| A. | HSO3-的电离方程式:HSO3-+H2O?H2SO3+OH- | |
| B. | 用铜为电极电解饱和食盐水:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH- | |
| C. | 向CaCl2溶液中通入少量CO2气体:Ca2++CO2+H2O═CaCO3↓+2H+ | |
| D. | 向NaHSO4溶液中逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
分析 A.亚硫酸氢根离子在溶液中部分电离出氢离子和亚硫酸根离子,该反应为亚硫酸氢根离子的水解;
B.铜为电极,阳极铜失去电子,阴极水电离出的氢离子得到电子生成氢气,不会生成氯气;
C.氯化钙不与二氧化碳反应;
D.硫酸根离子恰好完全沉淀时,二者的物质的量之比为1:1,氢氧根离子有剩余.
解答 解:A.亚硫酸氢根离子在溶液中部分电离出氢离子和亚硫酸根离子,其正确的电离的离子方程式为:HSO3-?SO32-+H+,故A错误;
B.用铜为电极电解饱和食盐水,阳极铜放电,正确的离子方程式为:Cu+2H2O$\frac{\underline{\;通电\;}}{\;}$Cu(OH)2↓+H2↑,故B错误;
C.向CaCl2溶液中通入少量CO2气体,二者不发生反应,无法书写离子方程式,故C错误;
D.NaHSO4溶液中逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀,反应的离子方程式为:H++SO42-+Ba2++OH-═BaSO4↓+H2O,故D正确;
故选D.
点评 本题考查了离子方程式的书写判断,为中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.M、N、X、Y四种物质有如下转化关系,M$→_{反应①}^{X}$N$→_{反应②}^{X}$Y(反应条件和其他产物已省略),下列选项不可能的是( )
| A. | M:Na X:O2 | B. | M:IINO3 X:Fe | C. | M:NH3 X:O2 | D. | M:Al X:NaOH |
2.下列表示物质结构的化学用语或模型正确的是( )
| A. | 乙烯的结构简式:CH2CH2 | B. | CH4分子的比例模型: | ||
| C. | 8个中子的碳原子的符号:12C | D. | Cl-的结构示意图: |
9.下列实验设计或实验操作中,正确的是( )
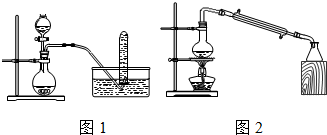

| A. | 铜与浓硝酸反应制取NO2可采用图1装置: | |
| B. | 图2实验装置设计正确,该装置可实现石油的分馏 | |
| C. | 分离乙酸和乙醇溶液:不能用分液漏斗进行分离 | |
| D. | 制乙酸乙酯时,把乙醇和乙酸依次加入浓硫酸中 |
7.下列有关气体摩尔体积的描述中正确的是( )
| A. | 在一定温度和压强下,单位物质的量的气体所占的体积就是气体摩尔体积 | |
| B. | 在0℃,1标准大气压下的气体摩尔体积约为22.4L | |
| C. | 标准状况下,1mol酒精的体积约为22.4L | |
| D. | 相同物质的量的气体,其体积也相同 |
 五种短周期元素A、B、C、D、E原子序数依次增大,结合下列信息:
五种短周期元素A、B、C、D、E原子序数依次增大,结合下列信息: ;
;