题目内容
在盛有稀H2SO4的烧杯中放入用导线连接的锌片和铜片,下列叙述正确的是
| A.正极附近的SO42-离子浓度逐渐增大 |
| B.电子通过导线由铜片流向锌片 |
| C.正极有O2逸出 |
| D.铜片上有H2逸出 |
D
解析试题分析:Zn、Cu、硫酸构成的原电池金属锌做负极,金属铜做正极。正极上放电的是氢离子,发生得电子的还原反应,氢离子浓度减少,SO42-离子向负极移动,所以SO42-离子浓度逐渐减少,故A错误;原电池中,电子的流向是从负极经导线流向正极,即从锌片流向铜片,故B错误;C、正极上放电的是氢离子,正极有氢气逸出,故C错误;金属铜做正极,正极上放电的是氢离子,有氢气逸出,故D正确。
考点:原电池
点评:本题考查原电池的基础知识,该考点是高考考查的重点和热点,本题难度不大。

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
 (2011?奉贤区一模)如图,在盛有稀 H2SO4 的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )
(2011?奉贤区一模)如图,在盛有稀 H2SO4 的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )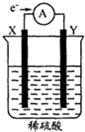 如图,在盛有稀H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示.下列关于该装置的判断正确的是( )
如图,在盛有稀H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示.下列关于该装置的判断正确的是( )