题目内容
5.下列各项括号内为杂质,后面为除杂质操作,其中正确的是( )| A. | 溴苯(液溴),加四氯化碳、萃取 | |
| B. | 乙烷(乙烯),通入高锰酸钾溶液、洗气 | |
| C. | 溴乙烷(乙醇),加水振荡、分液 | |
| D. | 乙酸乙酯(乙酸),加氢氧化钠溶液振荡、分液 |
分析 A.溴苯和溴都易溶于四氯化碳;
B.乙烯被氧化生成二氧化碳气体;
C.乙醇易溶于水;
D.乙酸乙酯和乙酸都能与氢氧化钠反应.
解答 解:A.溴苯和溴都易溶于四氯化碳,无法分开,故A错误;
B.乙烯被氧化生成二氧化碳气体,应用溴水除杂,故B错误;
C.乙醇易溶于水,溴乙烷不溶于水,可用分液分开,故C正确;
D.乙酸乙酯和乙酸都能与氢氧化钠反应,将原物质除掉,应用饱和碳酸钠分液,故D错误.
故选C.
点评 本题考查物质的分离和提纯,为高考常见题型,侧重于学生的分析能力和实验能力的考查,难度不大,注意把握物质的性质的异同.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.A、B、C、D四种元素,已知A元素是地壳中含量最多的元素;B元素为金属元素,它的原子核外K、L层上电子数之和等于M、N层电子数之和;C元素是第3周期第一电离能最小的元素;D元素在第3周期中第一电离能最大.下列有关叙述错误的是( )
| A. | 四种元素A、B、C、D分别为O、Ca、Na、Ar | |
| B. | 元素A、B、C两两组成的化合物可为CaO、CaO2、Na2O、Na2O2等 | |
| C. | 元素A、C简单离子的半径大小关系为A<C | |
| D. | 元素B、C的单质与水都能剧烈反应 |
20.下列说法正确的是(NA表示阿伏加德罗常数的值)( )
| A. | 1 mol聚乙烯含有的原子数目为6NA | |
| B. | 标准状况下,11.2L CHCl3中所含有的原子总数为2.5NA | |
| C. | 一定条件下,2.6 g乙炔、苯的气态混合物中所含碳原子数为0.2NA | |
| D. | 1 mol甲基与1mol羟基所含电子数均为10 NA个 |
15.下列用来表示物质变化的化学用语中,正确的是( )
| A. | 钢铁发生电化学腐蚀的正极反应式:Fe-2e-=Fe2+ | |
| B. | HS-水解的离子方程式:HS-+H2O?S2-+H3O+ | |
| C. | CO32-水解的离子方程式:CO32-+2 H2O?H2CO3+2OH- | |
| D. | 用FeS为沉淀剂除去废水中的Hg2+:FeS(s)+Hg2+(aq)=HgS(s)+Fe2+(aq) |
 .
. .
. .
. (1)明矾可用于净水,用离子方程式解释其原因Al3++3H2O?Al(OH)3(胶体)+3H+.把FeCl3溶液蒸干、灼烧、最后得到的主要固体产物是Fe2O3.
(1)明矾可用于净水,用离子方程式解释其原因Al3++3H2O?Al(OH)3(胶体)+3H+.把FeCl3溶液蒸干、灼烧、最后得到的主要固体产物是Fe2O3.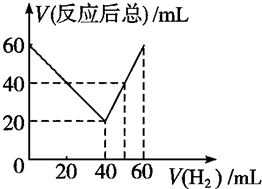 某气态不饱和链烃CnHm在一定条件下与H2加成为CnHm+x,取CnHm和H2混合气体共60mL进行实验,发现随混合气中H2所占体积的变化,反应后得到的气体总体积数也不同,反应前混合气体中H2所占的体积V(H2)和反应后气体总体积V(反应后总)的关系如图所示(气体体积均在同温同压下测定).由此可知x的数值为( )
某气态不饱和链烃CnHm在一定条件下与H2加成为CnHm+x,取CnHm和H2混合气体共60mL进行实验,发现随混合气中H2所占体积的变化,反应后得到的气体总体积数也不同,反应前混合气体中H2所占的体积V(H2)和反应后气体总体积V(反应后总)的关系如图所示(气体体积均在同温同压下测定).由此可知x的数值为( )