题目内容
19.制备FeSO4最适宜的方法是( )| A. | 过量的铁与稀H2SO4反应 | B. | FeO与H2SO4反应 | ||
| C. | FeCO3与H2SO4稀反应 | D. | Fe(OH)3与稀H2SO4反应 |
分析 A.无论Fe是否过量,Fe和稀硫酸都只生成硫酸亚铁;
B.FeO和稀硫酸反应生成硫酸亚铁和水;
C.碳酸铁和稀硫酸反应生成硫酸亚铁、二氧化碳和水;
D.氢氧化铁和稀硫酸反应生成硫酸铁和水.
解答 解:A.无论Fe是否过量,Fe和稀硫酸都只生成硫酸亚铁,过量的Fe和稀硫酸反应生成硫酸亚铁和氢气,且稀硫酸没有剩余,所以该方法制备较适宜,故A选;
B.FeO和稀硫酸反应生成硫酸亚铁和水,稀硫酸如果过量导致溶液中溶质有两种,故B不选;
C.碳酸铁和稀硫酸反应生成硫酸亚铁、二氧化碳和水,如果稀硫酸过量导致溶液中溶质有两种,故C不选;
D.氢氧化铁和稀硫酸反应生成硫酸铁和水,如果稀硫酸过量,导致溶液中溶质有两种,故D不选;
故选A.
点评 本题以物质制备为载体考查化学实验方案评价,为高频考点,明确物质性质及物质量的多少是解本题关键,为易错题.

练习册系列答案
相关题目
9.下列关于物质的性质或应用说法正确的是( )
| A. | 钠与乙醇反应比与水反应剧烈 | |
| B. | 常温下可用铝制容器贮存稀硝酸 | |
| C. | 干燥的氯气具有漂白性 | |
| D. | 用氯化铁溶液与铜反应制印刷电路板 |
10.下列物质里含氢原子数最多的是( )
| A. | 1 mol H2 | B. | 0.5molNH3 | ||
| C. | 6.02×1023个的CH4分子 | D. | 29.4gH3PO4 |
7.同温同压下,相同体积的CO和CO2的下列比较中正确的是( )
①所含的分子数目之比为1:1 ②所含的O原子数目之比为1:2
③所含的原子总数目之比为2:3④两者的密度之比为:7:11
⑤所含的电子数目之比为7:11.
①所含的分子数目之比为1:1 ②所含的O原子数目之比为1:2
③所含的原子总数目之比为2:3④两者的密度之比为:7:11
⑤所含的电子数目之比为7:11.
| A. | ①和④ | B. | ②和③ | C. | ④和⑤ | D. | ①②③④⑤ |
14.有一块重36g的薄铁片.将它浸入160g CuSO4溶液中,一段时间后取出铁片洗净后称量,其质量为39.2g.则溶液中Fe2+的物质的量为( )
| A. | 0.45mol | B. | 0.35mol | C. | 0.4mol | D. | 无法计算 |
10.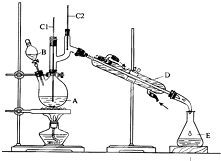 正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.
正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.
发生的反应如下:CH3CH2CH2CH2OH$→_{H_{2}SO_{4}△}^{Na_{2}Cr_{2}O_{7}}$CH3CH2CH2CHO
反应物和产物的相关数据列表如下:
实验步骤如下:
将Na2Cr2O7溶液与浓硫酸混合液放置在B中.在A中加入正丁醇和几粒沸石,加热,保持反应温度为90~95℃,在E中收集90℃以上的馏分.
将馏出物倒入分液漏斗中,除去水层,有机层干燥后蒸馏,收集75~77℃馏分.
回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,说明理由不能,容易发生迸溅.
(2)上述装置图中,B仪器的名称是分液漏斗,D仪器的名称是直形冷凝管.
(3)温度计的作用分别是C1C1控制反应温度;C2C2测定蒸馏出来气体的温度.
(4)将正丁醛粗产品置于分液漏斗中水在下层(填“上”或“下”).
(5)反应温度应保持在90~95℃,其原因是既可保证正丁醛及时蒸出,又可尽量避免其被进一步氧化.
 正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.
正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.发生的反应如下:CH3CH2CH2CH2OH$→_{H_{2}SO_{4}△}^{Na_{2}Cr_{2}O_{7}}$CH3CH2CH2CHO
反应物和产物的相关数据列表如下:
| 沸点/℃ | 密度/g•cm-3 | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
将Na2Cr2O7溶液与浓硫酸混合液放置在B中.在A中加入正丁醇和几粒沸石,加热,保持反应温度为90~95℃,在E中收集90℃以上的馏分.
将馏出物倒入分液漏斗中,除去水层,有机层干燥后蒸馏,收集75~77℃馏分.
回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,说明理由不能,容易发生迸溅.
(2)上述装置图中,B仪器的名称是分液漏斗,D仪器的名称是直形冷凝管.
(3)温度计的作用分别是C1C1控制反应温度;C2C2测定蒸馏出来气体的温度.
(4)将正丁醛粗产品置于分液漏斗中水在下层(填“上”或“下”).
(5)反应温度应保持在90~95℃,其原因是既可保证正丁醛及时蒸出,又可尽量避免其被进一步氧化.
8.下列反应的离子方程式书写正确的是( )
| A. | Fe0溶于稀硝酸:FeO+2H+═Fe2++H2O | |
| B. | 明矾溶液中滴加过量氨水:Al3++3NH3.H2O═Al(OH)3↓+3NH${\;}_{4}^{+}$ | |
| C. | 漂白粉溶液中通入S02:Ca2++2ClO-+SO2+H2O═2HClO+CaSO3↓ | |
| D. | 小苏打溶液中加足量澄清石灰水:2HCO${\;}_{3}^{-}$+Ca2++2OH-═CaCO3↓+2H2O+CO${\;}_{3}^{2-}$ |
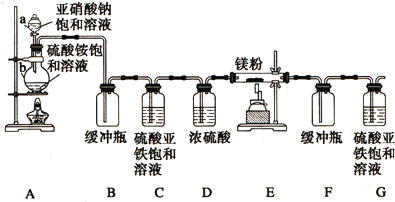
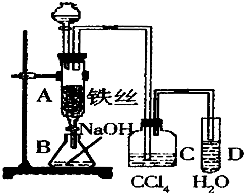 某化学课外小组用如图装置制取溴苯.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中.
某化学课外小组用如图装置制取溴苯.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中.