题目内容
已知pH=13的NaOH溶液,稀释100倍,求稀释后溶液pH?
解析:
|
[=J]pH=13,c(H+)=1×10-13 mol·L-1, c(OH-)= 稀释100倍:c(H+)= pH=-lg{c(H+)}=-lg1×10-11=11. 强碱溶液,当体积扩大100倍,溶液中c(OH-)减少100倍,pH降低2. 总结:强酸(弱碱),弱酸(强碱)加水稀释后的pH变化规律: (1)强酸,pH=a,加水稀释10n倍,则pH=a+n; (2)弱酸,pH=a,加水稀释10n倍,则pH<a+n; (3)强碱,pH=b,加水稀释10n倍,则pH=b-n; (4)弱碱,pH=b,加水稀释10n倍,则pH>b-n; (5)酸碱无限稀释,pH只能接近于7,酸不可能大于7,碱不可能小于7. 两个单位,由13变为11.溶液中c(OH-)减少,c(H+)增大,pH变小. |

 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
(1)B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确?___________(选填“是”或“否”)。若不正确,则二者恰好完全反应的点是在AB区间还是BD区间内?___________区间(若正确,此问不答)。
(2)关于该滴定实验,从下列选项中选出最恰当的一项___________。(选填字母)

| 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 | 选用滴定管 |
A | 碱 | 酸 | 石蕊 | (乙) |
B | 酸 | 碱 | 甲基橙 | (甲) |
C | 碱 | 酸 | 酚酞 | (甲) |
D | 酸 | 碱 | 酚酞 | (乙) |
(3)AB区间,c(OH-)>c(H+),则c(OH-)与c(CH3COO-)大小关系是________。
A.c(OH-)一定大于c(CH3COO-) B.c(OH-)一定小于c(CH3COO-)
C.c(OH-)一定等于c(CH3COO-) D.c(OH-)大于、小于或等于c(CH3COO-)
(4)在D点时,溶液中c(CH3COO-)+c(CH3COOH)___________2c(Na+)。(填“>”“<”或“=”)
Ⅱ.t ℃时,某稀硫酸溶液中c(H+)=10-a mol·L-1,c(OH-)=10-b mol·L-1,已知a+b=13:
(5)该温度下水的离子积常数KW的数值为___________。
(6)该温度下(t ℃),将100 mL 0.1 mol·L-1的稀硫酸溶液与100 mL 0.4 mol·L-1的NaOH溶液混合后(溶液体积变化忽略不计),溶液的pH=___________。
 HCO3-+H+的平衡常数K1=________.(已知:10-5.60=2.5×10-6)
HCO3-+H+的平衡常数K1=________.(已知:10-5.60=2.5×10-6)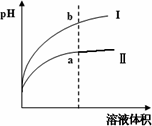
 HCO3-+H+的平衡常数K1= 。(已知:10-5.60=2.5×10-6)
HCO3-+H+的平衡常数K1= 。(已知:10-5.60=2.5×10-6)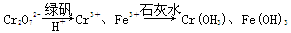
 HCO3-+H+的平衡常数K1=
。(已知:10-5.60=2.5×10-6)
HCO3-+H+的平衡常数K1=
。(已知:10-5.60=2.5×10-6)