题目内容
某温度下,把3molA和2.5molB混合,盛入容积为2L的容器内,使它们发生反应:
3A(气)+B(气) xC(气)+2D(气)
xC(气)+2D(气)
经过5min后达到平衡生成1mol D , 测得C的平均生成速率为0.10mol·L-1·min-1。下列叙述不正确的是
A.x的值为2
B.B的转化率为20%
C.平衡常数为1/3
D.A的平均消耗速率为0.15mol·L-1·min-1
【答案】
C
【解析】
试题分析:选写出分析式:
3A(气)+B(气) xC(气)+2D(气)
xC(气)+2D(气)
n开始/mol 3 2.5
n变化/mol ―1.5 ―0.5 +X/2 +1
n平衡/mol 1.5 2 X/2 1
A、C的平均生成速率为0.10mol·L-1·min-1 =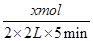 ,解得x=2,A正确;B、B的转化率为0.5mol/2.5mol×100%=20%,B正确;C、平衡常数
,解得x=2,A正确;B、B的转化率为0.5mol/2.5mol×100%=20%,B正确;C、平衡常数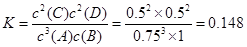 ,C不正确;D、A的平均消耗速率为=
,C不正确;D、A的平均消耗速率为=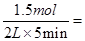 0.15mol·L-1·min-1
,D正确。选C。
0.15mol·L-1·min-1
,D正确。选C。
考点 :化学反应速率与化学平衡计算

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 把1 mol CO2和3mol H2通入1 L的密闭容器中,在某温度下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1
把1 mol CO2和3mol H2通入1 L的密闭容器中,在某温度下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1测得CO2和CH3OH的浓度随时间变化如图所示,下列说法正确的是( )
| A、3min时,v正=v逆 | B、0~10 min内,氢气的平均反应速率为0.225 mol?L-1?min-1 | C、该温度下,反应的平衡常数K=5.3 mol-2?L2 | D、若升高温度,CO2的平衡转化率大于75% |
 此条件下,该反应达到化学平衡时,氮气的浓度为
此条件下,该反应达到化学平衡时,氮气的浓度为
