题目内容
下列实验过程中,始终没有明显现象现象的是( )
| A、向Fe(OH)3胶体中逐滴滴加入过量稀H2SO4 |
| B、CO2通入CaCl2溶液中 |
| C、NH3通入AlCl3溶液中 |
| D、SO2通入已酸化的Ba(NO3)2溶液中 |
考点:胶体的重要性质,氨的化学性质,二氧化硫的化学性质,镁、铝的重要化合物
专题:元素及其化合物
分析:A.根据胶体的性质判断,加入稀硫酸产生聚沉现象,H2SO4与Fe(OH)3反应,所以出现先沉淀后溶解现象;
B.碳酸比盐酸弱,CO2与CaCl2溶液不会反应;
C.氯化铝和一水合氨反应生成氢氧化铝沉淀和氯化铵,氢氧化铝不溶于弱碱;
D.硝酸根能够氧化二氧化硫生成硫酸根,硫酸根与钡离子反应生成硫酸钡.
B.碳酸比盐酸弱,CO2与CaCl2溶液不会反应;
C.氯化铝和一水合氨反应生成氢氧化铝沉淀和氯化铵,氢氧化铝不溶于弱碱;
D.硝酸根能够氧化二氧化硫生成硫酸根,硫酸根与钡离子反应生成硫酸钡.
解答:
解:A.向Fe(OH)3胶体中加入H2SO4会出现先凝聚生成Fe(OH)3沉淀,H2SO4过量,Fe(OH)3与H2SO4反应而溶解,故A不选;
B.碳酸比盐酸弱,CO2与CaCl2溶液不会反应,无沉淀生成,故选B;
C.氢氧化铝不溶于弱碱一水合氨,向AlCl3溶液加入NH3?H2O溶液中生成Al(OH)3沉淀,故C不选;
D.硝酸根能够氧化二氧化硫生成硫酸根,硫酸根与钡离子反应生成硫酸钡,故D不选;
故选B.
B.碳酸比盐酸弱,CO2与CaCl2溶液不会反应,无沉淀生成,故选B;
C.氢氧化铝不溶于弱碱一水合氨,向AlCl3溶液加入NH3?H2O溶液中生成Al(OH)3沉淀,故C不选;
D.硝酸根能够氧化二氧化硫生成硫酸根,硫酸根与钡离子反应生成硫酸钡,故D不选;
故选B.
点评:本题综合考查元素化合物知识,为高考常见题型,侧重于元素化合价知识的综合理解和运用的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
下列物质中属于纯净物的是( )
①由同种元素组成的物质
②具有固定熔沸点的物质
③只有一种元素的阳离子和另一种元素的阴离子组成的物质
④在氧气中燃烧只生成二氧化碳的物质
⑤只含有一种分子的物质.
①由同种元素组成的物质
②具有固定熔沸点的物质
③只有一种元素的阳离子和另一种元素的阴离子组成的物质
④在氧气中燃烧只生成二氧化碳的物质
⑤只含有一种分子的物质.
| A、①③ | B、③④⑤ | C、②⑤ | D、②④ |
用R代表短周期元素,R原子最外层的p能级上的未成对电子只有2个.下列关于R的描述中正确的是( )
| A、R的氧化物都能溶于水 |
| B、R都是非金属元素 |
| C、R的氧化物都能与NaOH反应 |
| D、R的最高价氧化物对应的水化物都是H2RO3 |
下列叙述中,不正确的是( )
①原子晶体中只含有极性键
②金属在常温时都以晶体形式存在
③离子晶体一定含离子键,也可能有共价键
④分子晶体中一定有分子间作用力,有的还可能有氢键.
①原子晶体中只含有极性键
②金属在常温时都以晶体形式存在
③离子晶体一定含离子键,也可能有共价键
④分子晶体中一定有分子间作用力,有的还可能有氢键.
| A、①④ | B、②③ | C、①② | D、①③ |
下列物质属于共价化合物的是( )
| A、KOH |
| B、MgO |
| C、H2O |
| D、N2 |
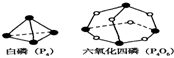 化学反应可视为旧键的断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol 化学键时释放(或吸收)出的能量.已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(KJ?mol-1)P-P:198 P-O:360 O=O:498 则反应P4(白磷)+3O2→P4O6 的反应热△H为( )
化学反应可视为旧键的断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol 化学键时释放(或吸收)出的能量.已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(KJ?mol-1)P-P:198 P-O:360 O=O:498 则反应P4(白磷)+3O2→P4O6 的反应热△H为( )| A、+1638KJ?mol-1 |
| B、-1638KJ?mol-1 |
| C、+126KJ?mol-1 |
| D、-126KJ?mol-1 |
化学反应前后可能发生变化的是( )
| A、物质的总质量 | B、元素种类 |
| C、原子数目 | D、分子数目 |
下列离子方程正确的是( )
| A、向氢氧化钙溶液中通入足量二氧化碳 OH-+CO2═HCO3- |
| B、向稀硫酸溶液中投入铁粉 2Fe+6H+═2Fe3++3H2↑ |
| C、向盐酸中投入碳酸钙 CO32-+2H+═H2O+CO2↑ |
| D、氢氧化钡溶液中加入硫酸 H++OH-═H2O |