题目内容
【题目】白磷和氯气反应生成PCl3的热化学方程式为P4(白磷,g)+6Cl2(g)═4PCl3(g) ΔH=-1326kJ·mol-1,已知化学键键能为Cl—Cl键243kJ·mol-1,P—Cl键331kJ·mol-1。白磷和PCl3的分子结构如图所示,则P—P键的键能为( )
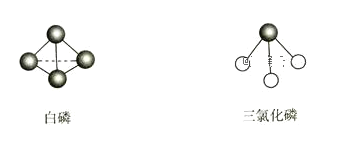
A.396kJ·mol-1B.198kJ·mol-1
C.99kJ·mol-1D.49.5kJ·mol-1
【答案】B
【解析】
已知反应的ΔH=反应物的键能和-生成物的键能和,设P—P键的键能为x,则P4(白磷,g)+6Cl2(g)═4PCl3(g) ΔH=-1326kJ·mol-1=(x)×6+(243kJ·mol-1)×6-(331kJ·mol-1)×4×3,解得:x=198kJ·mol-1, 故答案为B。

【题目】为测定碱式碳酸钴[COx(OH)y(CO3)z]的化学组成,研究性学习小组的同学设计了如图所示的装置进行实验探究。已知:碱式碳酸钴受热时可分解生成三种氧化物。
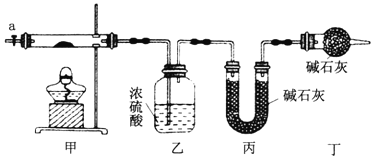
(1)按如图所示装置组装好仪器,并___________;称取3.65g样品置于硬质玻璃管内,加热,当乙装置中_______(填实验现象),停止加热;打开活塞a,缓缓通入空气数分钟,通入空气的目的是__________。
(2)某同学认为上述实验中存在一个缺陷,该缺陷是_________。
(3)通过正确实验测得乙、丙装置增重分别为0.36g、0.88g,则该碱式碳酸钴的化学式为__________。
(4)CoCl2·6H2O常用作多彩水泥的添加剂。以含钴废料(含少量Fe、Al等杂质)制取COCl2·6H2O的一种工艺如下:
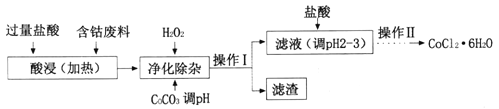
已知:25℃时
沉淀物 | Fe(OH)3 | Fe(OH)2 | CO(OH)2 | Al(OH)3 |
开始沉淀(pH) | 2.3 | 7.5 | 7.6 | 3.4 |
完全沉淀(pH) | 4.1 | 9.7 | 9.2 | 5.2 |
①净化除杂时,加入H2O2发生反应的离子方程式为______________;
②加入CoCO3调pH为5.2~7.6,则操作I获得的滤渣成分为_________;
③加盐酸调整pH为2~3的目的为___________;
④操作Ⅱ过程为蒸发浓缩、冷却结晶、过滤。



