题目内容
下列叙述不正确的是( )A.用反应热数据的大小判断不同反应的反应速率的快慢
B.用pH数据推测相同浓度的不同强酸弱碱盐在水溶液中水解程度的大小
C.应用盖斯定律,可计算某些难以直接测量的反应焓变
D.用平衡常数的大小判断化学反应可能进行的程度
【答案】分析:A、影响反应速率的是活化能,而不是反应热;只能确定反应的可能性;
B、依据盐类水解显示的酸碱性,比较不同强酸弱碱盐在水溶液中水解程度的大小;
C、化学反应的焓变不能逐个实验测定,应用盖斯定律可以计算某些反应的焓变;
D、平衡常数是衡量化学平衡进行程度的量,平衡常数越大,反应进行程度越大;
解答:解:A、反应热的大小和反应速率无直接影响,吸热的反应可能很快发生(铵盐与碱),放热的反应也可以很慢(常温下氢气和氧气反应),故A错误;
B、用pH数据推测相同浓度的不同强酸弱碱盐在水溶液中水解程度的大小,PH越小说明水解程度越大;故B正确;
C、应用盖斯定律,可计算某些难以直接测量的反应焓变,反应和起始物质和终了物质能量有关,与变化过程无关,故C正确;
D、平衡常数是衡量化学平衡进行程度的量,用平衡常数的大小判断化学反应可能进行的程度大小,故D正确;
故选A.
点评:本题考查了反应热和速率关系理解,溶液PH判断盐类水解的程度大小,盖斯定律的应用,平衡常数的含义,题目难度中等.
B、依据盐类水解显示的酸碱性,比较不同强酸弱碱盐在水溶液中水解程度的大小;
C、化学反应的焓变不能逐个实验测定,应用盖斯定律可以计算某些反应的焓变;
D、平衡常数是衡量化学平衡进行程度的量,平衡常数越大,反应进行程度越大;
解答:解:A、反应热的大小和反应速率无直接影响,吸热的反应可能很快发生(铵盐与碱),放热的反应也可以很慢(常温下氢气和氧气反应),故A错误;
B、用pH数据推测相同浓度的不同强酸弱碱盐在水溶液中水解程度的大小,PH越小说明水解程度越大;故B正确;
C、应用盖斯定律,可计算某些难以直接测量的反应焓变,反应和起始物质和终了物质能量有关,与变化过程无关,故C正确;
D、平衡常数是衡量化学平衡进行程度的量,用平衡常数的大小判断化学反应可能进行的程度大小,故D正确;
故选A.
点评:本题考查了反应热和速率关系理解,溶液PH判断盐类水解的程度大小,盖斯定律的应用,平衡常数的含义,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
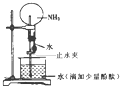 如图是实验室进行氨溶于水的“喷泉实验”的装置,下列叙述不正确的是( )
如图是实验室进行氨溶于水的“喷泉实验”的装置,下列叙述不正确的是( )| A、该实验说明氨气是一种极易溶于水的气体 | B、进入烧瓶中的液体颜色由无色变为红色,说明氨水有碱性 | C、氨水很稳定,将烧瓶中的红色溶液加热,颜色不会发生变化 | D、形成“喷泉”的主要原因是氨气溶于水后,烧瓶内的气压小于大气压 |
苯与乙烯相比较,下列叙述不正确的是( )
| A、都能燃烧,生成二氧化碳和水 | B、都容易发生加成反应 | C、乙烯易发生加成反应,苯只能在特殊条件下才发生加成反应 | D、乙烯易被酸性高锰酸钾溶液氧化,苯不能被酸性高锰酸钾溶液氧化 |