题目内容
 如图所示,是实验室制备某常见气体的实验装置,请填空:
如图所示,是实验室制备某常见气体的实验装置,请填空:(1)该实验装置制备的常见气体是(填写化学式):
NH3
NH3
.(2)制备该气体的化学方程式是:
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
| ||
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O
.
| ||
(3)收集该气体的方法是:
向下排空气法
向下排空气法
.(4)检验该气体是否收集满的方法是:
用湿润的红色石蕊试纸靠近试管口,若变蓝,则说明收集满
用湿润的红色石蕊试纸靠近试管口,若变蓝,则说明收集满
.(5)将充满该气体的试管倒立于水槽中,可以看到的现象是:
试管内液面上升
试管内液面上升
.分析:(1)实验室常用加热固体的方法制取氨气,根据反应物状态和反应条件选取装置.
(2)根据反应物和生成物及反应条件写出反应方程式.
(3)氨气极易溶于水,且氨气和氧气在常温条件下不反应,所以采用排空气法收集,根据氨气和空气密度的相对大小确定采用哪种排空气法收集.
(4)氨气是碱性气体,能使湿润的红色石蕊试纸变蓝.
(5)氨气极易溶于水,根据试管内气体的压强变化确定看到的现象.
(2)根据反应物和生成物及反应条件写出反应方程式.
(3)氨气极易溶于水,且氨气和氧气在常温条件下不反应,所以采用排空气法收集,根据氨气和空气密度的相对大小确定采用哪种排空气法收集.
(4)氨气是碱性气体,能使湿润的红色石蕊试纸变蓝.
(5)氨气极易溶于水,根据试管内气体的压强变化确定看到的现象.
解答:解:(1)实验室常用加热固体氯化铵和氢氧化钙的方法制取氨气,选用的反应装置是固体混合加热型装置,所以该装置制备的常见气体是NH3.
故答案为:NH3.
(2)反应方程式为2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O.
故答案为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O.
(3)氨气极易溶于水,所以不能采用排水法收集气体;常温下氨气和氧气不反应,氨气的密度小于空气的密度,所以可以采用向下排空气法收集氨气.
故答案为:向下排空气法.
(4)氨气的碱性气体,能使湿润的红色石蕊试纸变蓝,所以检验氨气时用湿润的红色石蕊试纸靠近试管口,若变蓝,则说明收集满.
故答案为:用湿润的红色石蕊试纸靠近试管口,若变蓝,则说明收集满.
(5)氨气极易溶于水,将充满该气体的试管倒立于水槽中,氨气溶于水导致试管内气体压强变小,水进入试管内,所以可以看到的现象是试管内液面上升.
故答案为:试管内液面上升.
故答案为:NH3.
(2)反应方程式为2NH4Cl+Ca(OH)2
| ||
故答案为:2NH4Cl+Ca(OH)2
| ||
(3)氨气极易溶于水,所以不能采用排水法收集气体;常温下氨气和氧气不反应,氨气的密度小于空气的密度,所以可以采用向下排空气法收集氨气.
故答案为:向下排空气法.
(4)氨气的碱性气体,能使湿润的红色石蕊试纸变蓝,所以检验氨气时用湿润的红色石蕊试纸靠近试管口,若变蓝,则说明收集满.
故答案为:用湿润的红色石蕊试纸靠近试管口,若变蓝,则说明收集满.
(5)氨气极易溶于水,将充满该气体的试管倒立于水槽中,氨气溶于水导致试管内气体压强变小,水进入试管内,所以可以看到的现象是试管内液面上升.
故答案为:试管内液面上升.
点评:本题考查了氨气的制取、收集和性质等知识点,会根据物质的性质选取反应装置、洗气装置和收集装置.

练习册系列答案
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目
由于Fe(OH)2极易被氧化,所以实验室难用亚铁盐
溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.若用如图所
示实验装置可制得纯净的Fe(OH)2沉淀.两极材料分别为石
墨和铁。
(1)a电极材料为 ,其电极反应式为 。
(2)若电解液d是 (填字母编号,下同),则白色沉淀在电极上生成;若是 ,则白色沉淀在两极之间的溶液中生成。
| A.纯水 | B.NaCl溶液 | C.NaOH溶液 | D.CuCl2溶液 |
(4)若装置中生成的气体在标准状况下的体积为2.24L,则生成的沉淀质量为 g。
 如图所示装置是化学实验中常见的仪器,它除用于洗气外,还有其它用途.
如图所示装置是化学实验中常见的仪器,它除用于洗气外,还有其它用途.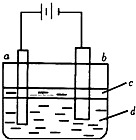 由于Fe(OH)2极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.
由于Fe(OH)2极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.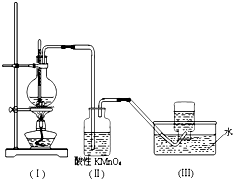 如图所示,在实验室里,通常利用浓硫酸与乙醇混合加热制乙烯,加热一段时间后观察到烧瓶中溶液变黑,装置(Ⅱ)中经硫酸酸化的高锰酸钾溶液褪色.
如图所示,在实验室里,通常利用浓硫酸与乙醇混合加热制乙烯,加热一段时间后观察到烧瓶中溶液变黑,装置(Ⅱ)中经硫酸酸化的高锰酸钾溶液褪色.