题目内容
现代工业将煤炭气化,既可以提高燃料的利用率、减少CO、SO2等的排放,又可以扩大水煤气的广泛用途.
(1)
已知:2C(s)+O2(g)=2CO(g);ΔH1,2H2(g)+O2(g)=2H2O(g);ΔH2.则反应C(s)+H2O(g)![]() CO(g)+H2(g);
CO(g)+H2(g);
(2)CO
和H2在一定条件下合成甲醇的反应为:CO(g)+2H2(g)
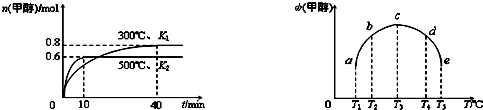
①该反应的ΔH3________0(选填“<”、“>”或“=”,下同),K1________K2.
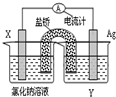
②将容器c中的平衡状态转变到容器d中的平衡状态,可采取的措施有________.
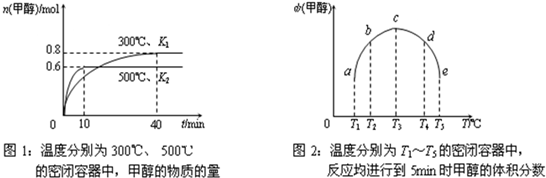
(3)某燃料电池以CO为燃料,以空气为氧化剂,以熔融态K2CO3为电解质.写出该燃料电池负极的电极反应式:________.
答案:
解析:
解析:
|
(1)(ΔH1-ΔH2)/2 (2)①< > ②升温或减压 (3)CO+CO |

练习册系列答案
 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目


 =_______,(用含
=_______,(用含 的代数式表示)
的代数式表示) ΔH3 。向容积均为1L的a, b、c、d、e五个密闭容器中分别充入1mol CO和2mol H2的混合气体,控温,进行实验,测得相关数据如下图1和图2。
ΔH3 。向容积均为1L的a, b、c、d、e五个密闭容器中分别充入1mol CO和2mol H2的混合气体,控温,进行实验,测得相关数据如下图1和图2。
 _______O (选填“<”、“>”或“=”)。
_______O (选填“<”、“>”或“=”)。