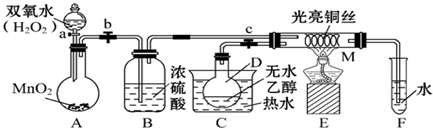
题目内容
14.下列说法中正确的是( )| A. | 全部由非金属元素组成的化合物中可能含有离子键 | |
| B. | 所有的单质中都含有化学键 | |
| C. | 只要化学键断裂了,一定有化学反应发生 | |
| D. | 分子是保持物质化学性质的一种微粒,且是化学变化中最小的微粒 |
分析 A.全部由非金属元素组成的化合物为共价化合物或离子化合物;
B.稀有气体的单质中不存在化学键;
C.化学键断裂和生成的变化为化学变化;
D.原子为化学变化中的最小微粒.
解答 解:A.全部由非金属元素组成的化合物为共价化合物或离子化合物,如HCl为共价化合物,氯化铵为离子化合物,故A正确;
B.稀有气体的单质中不存在化学键,多原子构成的单质中一定含化学键,故B错误;
C.化学键断裂和生成的变化为化学变化,只有化学键的断裂不一定发生化学变化,如电离,故C错误;
D.原子为化学变化中的最小微粒,分子是保持物质化学性质的一种微粒,故D错误;
故选A.
点评 本题考查化学键,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,注意结合实例分析,题目难度不大.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
4.下列元素中,最高正化合价数值最大的是( )
| A. | C | B. | Al | C. | S | D. | Ne |
19.如图为元素周期表短周期中的一部分,有关元素X、Y、Z、M的说法错误的是( )
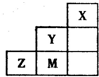

| A. | Y、Z可形成ZY6分子 | B. | X晶体属于原子晶体 | ||
| C. | 原子半径:Z>M>Y | D. | Z离子的结构示意图可表示为: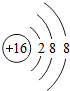 |
6.下列化学名词正确的是( )
| A. | 三溴笨酚 | B. | 烧碱 | C. | 硬脂酸甘油脂 | D. | 石碳酸 |
3.下列变化会放出热量的是( )
| A. | 碘升华 | B. | 冰融化 | C. | 氯化铵溶于水 | D. | 氢氧化钠溶于水% |
4.在H、O、C、Na四种元素中,选择适当的元素组成符合下列要求的物质,将它们的化学式填写在以下空格中.(注意:每种物质只能出现一次)
写出上述酸性氧化物和碱性氧化物发生化合反应的化学方程式:CO2+Na2O═Na2CO3
写出氯气与上述碱溶液发生反应的化学方程式:Cl2+2NaOH═NaCl+NaClO+H2O.
| 酸性氧化物 | 碱性氧化物 | 酸 | 碱 | 电解质 | 非电解质 |
写出氯气与上述碱溶液发生反应的化学方程式:Cl2+2NaOH═NaCl+NaClO+H2O.
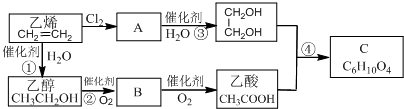
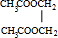 +2H2O.
+2H2O.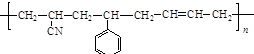 除苯乙烯外,还需要另外两种单体,写出这两种单体的结构简式CH2=CH-CN、CH2=CH-CH=CH2.
除苯乙烯外,还需要另外两种单体,写出这两种单体的结构简式CH2=CH-CN、CH2=CH-CH=CH2. )需要三步,第一步选用的试剂为HBr,目的是保护碳碳双键防止被加成.
)需要三步,第一步选用的试剂为HBr,目的是保护碳碳双键防止被加成.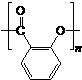 .
.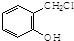 制备A的合成路线.
制备A的合成路线.