题目内容
表示下列微粒的电离方程式正确的是( )
| A、CuCl2═Cu2++Cl2- |
| B、HCO3-═H++CO32- |
| C、Fe2(SO4)3═2Fe2++3SO42- |
| D、Ba(NO3)2═Ba2++2(NO3)2- |
考点:电离方程式的书写
专题:离子反应专题
分析:A.物质电离后角标要转化成化学计量数;
B.碳酸氢根离子是多元弱酸碳酸的酸根离子,部分电离;
C.硫酸铁属于盐,属于强电解质,完全电离出硫酸根离子和铁离子;
D.硝酸钡电离出钡离子和硝酸根离子,硝酸根离子带一个单位负电荷;
B.碳酸氢根离子是多元弱酸碳酸的酸根离子,部分电离;
C.硫酸铁属于盐,属于强电解质,完全电离出硫酸根离子和铁离子;
D.硝酸钡电离出钡离子和硝酸根离子,硝酸根离子带一个单位负电荷;
解答:
解:A.氯化铜电离出铜离子和氯离子,物质电离后角标要转化成化学计量数,正确的离子方程式为:CuCl2═Cu2++2Cl-,故A错误;
B.碳酸氢根离子是多元弱酸碳酸的酸根离子,部分电离用“?”连接,正确的离子方程式为:HCO3-?H++CO32-,故B错误;
C.根据离子方程式的书写规则进行分析,该离子方程式离子书写正确,电荷守恒,故C正确;
D.硝酸钡属于强电解质,完全电离,硝酸根离子带一个单位负电荷,正确的离子方程式为:Ba(NO3)2═Ba2++2NO3-,故D错误;
故选C.
B.碳酸氢根离子是多元弱酸碳酸的酸根离子,部分电离用“?”连接,正确的离子方程式为:HCO3-?H++CO32-,故B错误;
C.根据离子方程式的书写规则进行分析,该离子方程式离子书写正确,电荷守恒,故C正确;
D.硝酸钡属于强电解质,完全电离,硝酸根离子带一个单位负电荷,正确的离子方程式为:Ba(NO3)2═Ba2++2NO3-,故D错误;
故选C.
点评:本题考查电离方程式的书写,掌握正确书写电离方程式的方法,并会正确判断离子方程式的正误是解答的关键,题目难度不大.

练习册系列答案
相关题目
将空气中氮气转化成氮的化合物的过程称为固氮.下列选项中能实现人工固氮的是( )
| A、闪电 | B、电解饱和食盐水车间 |
| C、根瘤菌 | D、合成氨车间 |
mA(g)+nB(g)?pC(g)+qQ(g)当m、n、p、q为任意整数时,达到平衡的标志是( )
①体系的压强不再改变
②体系的温度不再改变
③各组分的浓度不再改变
④各组分的质量分数不再改变
⑤反应速率VA:VB:VC:VD=m:n:p:q
⑥单位时间内m mol A断键反应,同时p mol C也断键反应.
①体系的压强不再改变
②体系的温度不再改变
③各组分的浓度不再改变
④各组分的质量分数不再改变
⑤反应速率VA:VB:VC:VD=m:n:p:q
⑥单位时间内m mol A断键反应,同时p mol C也断键反应.
| A、③④⑤⑥ | B、②③④⑥ |
| C、①③④⑤ | D、①③④⑥ |
在c(H+):c(OH-)=1:2的水溶液中能大量共存的离子组是( )
| A、K+、Al3+、HCO3-、SO42- |
| B、Ca2+、NH4+、CO32-、Cl- |
| C、Na+、K+、NO3-、ClO- |
| D、Na+、Fe2+、I-、SO32- |
下列叙述正确的是( )
| A、同周期元素中,ⅦA族元素的原子半径最大 |
| B、ⅠA族元素的原子,其半径越大,越容易得到电子 |
| C、室温时,零族元素的单质都是气体 |
| D、所有主族元素的原子,形成单原子离子时的化合价与它的族序数相等 |
化学用语在化学学科中作用非常重要,以下有关化学用语描述正确的是( )
A、Mg2+的结构示意图: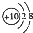 |
B、Na2S的电子式: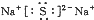 |
| C、氨气的空间结构:三角形 |
| D、乙烯的结构简式:(CH2)2 |
工业上制造玻璃时不需要用到的原料是( )
| A、纯碱石 | B、石灰 | C、石英 | D、食盐 |
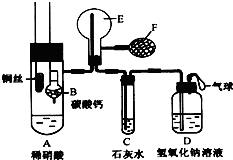 为了证明铜与稀硝酸反应产生的是NO,某校学生实验小组设计了一个实验,其装置如图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,
为了证明铜与稀硝酸反应产生的是NO,某校学生实验小组设计了一个实验,其装置如图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,