题目内容
5.多晶硅(硅单质的一种)被称为“微电子大厦的基石”,制备中副产物以SiCl4为主,它环境污染很大,能遇水强烈水解,放出大量的热.研究人员利用SiCl4水解生成的盐酸和钡矿粉(主要成分为BaCO3,且含有铁、镁等离子),制备BaCl2.2H2O,工艺流程如下:
已知:
①常温下Fe3+、Mg2+完全沉淀的PH分别是3.4、12.4;
②BaCO3的相对分子质量是197;BaCl2.2H2O的相对分子质量是244.
回答下列问题:
(1)SiCl4发生水解反应的化学方程式SiCl4+4H2O=H4SiO4↓+4HCl.
(2)SiCl4用H2还原可制取纯度很高的硅,当反应中有1mol电子转移时吸收59KJ热量,则该反应的热化学方程式为SiCl4(s)+2H2(g)=Si(s)+4HCl(g)△H=+236kJ/mol.
(3)加钡矿粉调节PH=7的作用是①使BaCO3转化为BaCl2②使Fe3+离子沉淀完全.
(4)生成滤渣A的离子方程式Mg2++2OH-=Mg(OH)2↓.
(5)BaCl2滤液经蒸发浓缩、冷却结晶、过滤、洗涤,再经真空干燥后得到BaCl2.2H2O
(6)10吨含78.8% BaCO3的钡矿粉理论上最多能生成BaCl2.2H2O9.76吨.
分析 四氯化硅控制温度40°C,加入水过滤得到原硅酸,则发生水解反应生成原硅酸和氯化氢,过滤得到盐酸溶液,加入钡矿粉主要成分为BaCO3,且含有铁、镁等离子,调节溶液pH=7,使BaCO3转化为BaCl2,同时使Fe3+完全沉淀,过滤得到滤渣为氢氧化铁,滤液加入氢氧化钠溶液调节溶液pH=12.5,控制70°C,得到氢氧化镁沉淀,过滤得到滤液为氯化钡溶液,再经过蒸发浓缩、冷却结晶、过滤、洗涤等得到氯化钡晶体.
(1)四氯化硅水解生成原硅酸和氯化氢;
(2)依据热化学方程式书写方法得到由SiCl4制备硅的热化学方程式,注意焓变的计算;
(3)由pH=3.4时,Fe3+离子转化为氢氧化铁,当调节PH=7时能促使Fe3+离子沉淀完全;
(4)滤液②中加入NaOH溶液调节溶液pH=12.5,溶液中镁离子与氢氧根离子反应生成氢氧化镁沉淀;
(5)从溶液中获得晶体,需要经过蒸发浓缩、冷却结晶、过滤、洗涤等;
(6)根据Ba元素质量守恒计算m(BaCl2•2H2O).
解答 解:四氯化硅控制温度40°C,加入水过滤得到原硅酸,则发生水解反应生成原硅酸和氯化氢,过滤得到盐酸溶液,加入钡矿粉主要成分为BaCO3,且含有铁、镁等离子,调节溶液pH=7,使BaCO3转化为BaCl2,同时使Fe3+完全沉淀,过滤得到滤渣为氢氧化铁,滤液加入氢氧化钠溶液调节溶液pH=12.5,控制70°C,得到氢氧化镁沉淀,过滤得到滤液为氯化钡溶液,再经过蒸发浓缩、冷却结晶、过滤、洗涤等得到氯化钡晶体.
(1)四氯化硅水解生成原硅酸和氯化氢,反应方程式为:SiCl4+4H2O=H4SiO4↓+4HCl,故答案为:SiCl4+4H2O=H4SiO4↓+4HCl;
(2)用H2还原SiCl4蒸气可制取纯度很高的硅,当反应中有1mol电子转移时吸收59KJ热量,转移4mol电子吸收热量236KJ,反应的热化学方程式:SiCl4(s)+2H2(g)=Si(s)+4HCl(g)△H=+236kJ/mol,
故答案为:SiCl4(s)+2H2(g)=Si(s)+4HCl(g)△H=+236kJ/mol;
(3)由pH=3.4时,Fe3+离子转化为氢氧化铁,当调节PH=7时能促使Fe3+离子沉淀完全,盐酸和碳酸钡反应生成氯化钡和二氧化碳、水,加钡矿粉并调节pH=7的作用是使BaCO3转化为BaCl2,使Fe3+离子沉淀完全,
故答案为:使Fe3+离子沉淀完全;
(4)滤液②中加入NaOH溶液调节溶液pH=12.5,溶液中镁离子与氢氧根离子反应生成氢氧化镁沉淀,反应离子方程式为:Mg2++2OH-=Mg(OH)2↓,
故答案为:Mg2++2OH-=Mg(OH)2↓;
(5)BaCl2滤液经蒸发浓缩、冷却结晶、过滤、洗涤,再经真空干燥后得到BaCl2•2H2O,故答案为:蒸发浓缩;冷却结晶;洗涤;
(6)根据Ba元素质量守恒:n(BaCl2•2H2O)=n(BaCO3),则m(BaCl2•2H2O)×=n(BaCl2•2H2O)×M(BaCl2•2H2O)=$\frac{10t×78%}{197g/mol}$×244g/mol=9.76t,
故答案为:9.76.
点评 本题考查制备实验方案、物质分离和提纯、对条件控制分析与评价、化学计算等,充分考查了学生的分析、理解能力及知识迁移运用的能力,难度中等.

| A. | 石英与烧碱反应:SiO2+2OH-═SiO32-+H2O | |
| B. | 硅与烧碱反应:Si+2OH-═SiO32-+H2↑ | |
| C. | 硅酸钠溶液中通入少量CO2:SiO32-+CO2+H2O═CO32-+H2SiO3↓ | |
| D. | 往水玻璃中加入盐酸:2H++SiO32-═H2SiO3↓ |
| A. | FeO、Fe2O3 | B. | FeO、Fe3O4 | C. | Fe2O3、Fe3O4 | D. | FeO、Fe2O3、Fe3O4 |
 图如中所示化合物A(fumimycin)是从微生物中分离得到的它显示出广谱抗菌活性.下列关于化合物A的说法中,正确的是( )
图如中所示化合物A(fumimycin)是从微生物中分离得到的它显示出广谱抗菌活性.下列关于化合物A的说法中,正确的是( )| A. | 该化合物A的分子式为:C15H15O6N | |
| B. | 化合物A可以水解得到2种有机物 | |
| C. | 化合物A可与 H2发生加成反应,1molA最多消耗H22mol | |
| D. | 化合物A与足量的溴水反应,1molA可以消耗5molBr2 |
| A. | SO2能使酸性KMnO4溶液褪色,故CO2也能使酸性KMnO4溶液褪色 | |
| B. | Mg与CuSO4反应置换出Cu,故Na与CuSO4反应也可以置换出Cu | |
| C. | 次氯酸可以令有色布条褪色,因其强氧化性,故过氧化钠也可以令有色布条褪色 | |
| D. | SO2能使品红溶液褪色,故CO2也能使品红溶液褪色 |
 金晶体是面心立方体,立方体的每个面5个金原子紧密堆砌(如图其余各面省略),金原子半径为1.44×10-10 m,Au的摩尔质量为197g/mol.求:
金晶体是面心立方体,立方体的每个面5个金原子紧密堆砌(如图其余各面省略),金原子半径为1.44×10-10 m,Au的摩尔质量为197g/mol.求:
 ,F:CH3CHO.
,F:CH3CHO. ,
, .
.

 ,
,
 的同分异构体:
的同分异构体: 、
、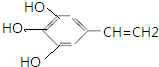 .
.