题目内容
2.格利雅试剂简称“格氏试剂”,它是卤代烃与金属镁在无水乙醚中作用得到的,它可与羰基发生加成反应,如:
今欲通过上述反应合成2-丙醇,选用的有机原料正确的一组是( )
| A. | 氯乙烷和甲醛 | B. | 氯乙烷和丙醛 | C. | 一氯甲烷和丙酮 | D. | 一氯甲烷和乙醛 |
分析 “格氏试剂”与羰基发生加成反应,其中的“-MgX”部分加到羰基的氧上,所得产物经水解可得醇,若合成(CH3)3C-OH,即2-甲基-2-丙醇,则反应物中碳原子数之和为4,结合产物中羟基的位置分析.
解答 解:由信息: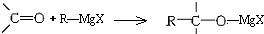 可知,此反应原理为断开C=O双键,烃基加在碳原子上,-MgX加在O原子上,产物水解得到醇,即发生取代反应,即氢原子(-H)取代-MgX,现要制取(CH3)3C-OH,即若合成2-甲基-2丙醇,则反应物中碳原子数之和为4,
可知,此反应原理为断开C=O双键,烃基加在碳原子上,-MgX加在O原子上,产物水解得到醇,即发生取代反应,即氢原子(-H)取代-MgX,现要制取(CH3)3C-OH,即若合成2-甲基-2丙醇,则反应物中碳原子数之和为4,
A、氯乙烷和甲醛反应生成产物经水解得到CH2(OH)CH2CH3,故A不选;
B、氯乙烷和丙醛反应生成产物经水解得到丁醇(CH3CH2CH(OH)CH2CH3),不是丙醇,故B不选;
C、一氯甲烷和丙酮反应生成产物经水解得到2-甲基-2-丙醇,不是2-丙醇,故C不选;
D、一氯甲烷和乙醛反应生成产物为2-丙醇,故D选;
故选D.
点评 本题考查有机物的结构和性质,侧重于学生的分析能力的考查,注意把握题给信息,把握官能团的性质,为解答该题的关键,答题时注意审题,难度中等.

练习册系列答案
相关题目
16.下列物质属于电解质的是( )
| A. | 氯化钠溶液 | B. | 酒精 | C. | 硫酸钠晶体 | D. | 二氧化碳 |
17.有三种化合物:①NaHCO3、②Al(OH)3、③H2NCH2COOH,跟盐酸和氢氧化钠溶液都能反应的是( )
| A. | 只有② | B. | 只有①② | C. | 只有②③ | D. | ①②③ |
10.最近日本科学家确认世界还存在着另一种“分子足球”N60,它与C60分子结构相似.N60在高温和撞击后会释放出巨大能量.下列对N60的说法不正确的是( )
| A. | N60和14N都是氮的同位素 | B. | N60和N2都是氮的同素异形体 | ||
| C. | N60中氮原子之间由共价键结合 | D. | N60高温和撞击后应该生成N2 |
17.NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 1.0L1.0mol•L-1的NaClO水溶液中含有的氧原子数为NA | |
| B. | 总质量为ag的CO和N2的混合物中所含原子总数为$\frac{a{N}_{A}}{14}$ | |
| C. | 2.24L 的2H35Cl分子中的中子数是1.9NA | |
| D. | 某密闭容器中盛有0.1mol N2和0.3molH2,在一定条件下充分反应,形成N-H键的数目为0.6NA |
7.A、B、C、D四种物质皆易溶于水,且室温下在水溶液(稀)中存在下列化学平衡,加入水稀释后恢复至室温,平衡正向移动的是( )
| A. | A+B+H2O?C+D | B. | A?C+D | C. | A+B?C+H2O | D. | A+2B+H2O?C |
14.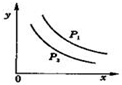 反应:L(s)+aG(g)?bR(g)达到平衡时,温度和压强对该反应的影响图所示:图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气中R的体积分数.据此可判断( )
反应:L(s)+aG(g)?bR(g)达到平衡时,温度和压强对该反应的影响图所示:图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气中R的体积分数.据此可判断( )
 反应:L(s)+aG(g)?bR(g)达到平衡时,温度和压强对该反应的影响图所示:图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气中R的体积分数.据此可判断( )
反应:L(s)+aG(g)?bR(g)达到平衡时,温度和压强对该反应的影响图所示:图中:压强p1>p2,x轴表示温度,y轴表示平衡混合气中R的体积分数.据此可判断( )| A. | 上述正反应是放热反应 | B. | 上述正反应是吸热反应 | ||
| C. | 增大L的量,平衡正向移动 | D. | a<b |
11.水凝结成冰的过程的焓变和熵变正确的是( )
| A. | △H>0,△S<0 | B. | △H<0,△S>0 | C. | △H>0,△S>0 | D. | △H<0,△S<0 |
12.下列图示的装置可以构成原电池的是( )
| A. | 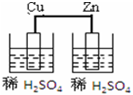 | B. | 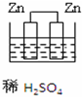 | C. | 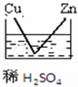 | D. | 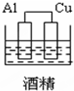 |