题目内容
A、B、C、D四种短周期元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,B与C的单质在加热条件下反应,生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层上的电子数之和.
(1)写元素符号:A为________,B为________,C为________.D的最高价氧化物的水化物化学式是________.
(2)写出A、B形成的化合物与E反应的化学方程式:________.
(3)E属________(“离子”或“共价”)化合物.E中含________键.
(4)D元素在周期表中位于第________周期________族.
答案:
解析:
解析:
|
(1)C O Na H2SO4. (2)2CO2+2Na2O2 (3)离子 离子键、共价键; (4)3 ⅥA |

练习册系列答案
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
A、B、C、D四种短周期元素的原子半径依次减小,A与C的核电荷数之比3:4,D分别与A、B、C可形成10个电子的分子X、Y、Z.则下列叙述正确的是( )
| A、X、Y、Z三种分子的稳定性逐渐减弱 | B、上述四种元素共能形成五种单质 | C、X、Y、Z三种分子的沸点逐渐升高 | D、X、Y、Z三种分子均为极性分子 |

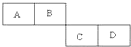 A、B、C、D四种短周期元素在周期表中的相对位置如表所示,A的单质与水蒸气反应可以制取水煤气.
A、B、C、D四种短周期元素在周期表中的相对位置如表所示,A的单质与水蒸气反应可以制取水煤气.