题目内容
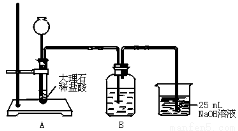
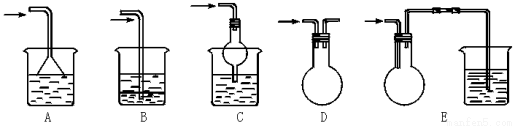
实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )

选项 | a中物质 | b中物质 | c中收集气体 | d中物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 浓硫酸 | 浓盐酸 | HCl | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
B
【解析】
试题分析:A、氨气的密度比空气小,不能使用向上排空气法,故A错误;B、浓盐酸在浓硫酸作用下生成HCl,HCl可用氢氧化钠溶液吸收,氢氧化钠极易溶于水,漏斗可以防止倒吸,密度比空气大,可用向上排空法收集,,故B正确;C、铜与稀硝酸反应需要加热,且产生的气体为NO,不能用排空气法收集,故C错误;D、制取氯气需要加热,氯气的密度比空气大,能使用向上排空气法,氯气用氢氧化钠溶液吸收时不需要防倒吸,故D错误;故选B。
考点:考查化学实验基本原理(气体的制备),实验装置、仪器的使用

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
下列事实不能用平衡移动原理解释的是( )
2SO2+O2 的平衡体系中,加入由18O构成的氧气,则SO2中的18O的含量会增加 |
|
|
| ||||||||||||
A | B | C | D |
 g/ml,质量分数为ω,物质浓度为c mol/L,则ρ=(17V+22400)/(22.4+22.4V)g/ml
g/ml,质量分数为ω,物质浓度为c mol/L,则ρ=(17V+22400)/(22.4+22.4V)g/ml mol/L
mol/L
 2SO3
2SO3

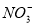

 ===BaCO3↓+CO
===BaCO3↓+CO +2H2O
+2H2O