��Ŀ����
����Ŀ����ͼ��ʵ������ȡSO2����֤SO2��ijЩ���ʵ�װ��(�г�װ�úͼ���װ�����ԣ��������Ѽ���)����ش��������⣺
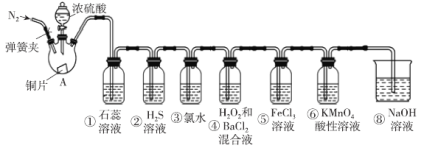
��1����A�з�����Ӧ�Ļ�ѧ����ʽΪ___��
��2�����е�ʵ������Ϊ��ɫʯ����Һ___��
���е�ʵ������Ϊ___��д���˻�ѧ��Ӧ����ʽ___��
���е�ʵ��������___��д���˻�ѧ��Ӧ����ʽ___��
���е�ʵ��������___��д���˻�ѧ��Ӧ����ʽ___��
���е���������Һ�ɻ�ɫ��Ϊdz��ɫ���䷴Ӧ�����ӷ���ʽΪ___��
��3�������ֳ�SO2��ԭ�Ե�ʵ�������___��
��4��ʵ���������Ҫͨ��N2����Ŀ����___��
���𰸡�Cu+2H2SO4![]() CuSO4+ SO2��+ 2H2O ��� ���ɻ�ɫ���� SO2+2H2S=S��+ 2H2O ��ˮ��ɫ SO2+Cl2+ 2H2O =2HCl+ H2SO4 �������ᱵ�İ�ɫ���� SO2+H2O2+BaCl2= BaSO4��+2HCl SO2+2Fe3++2H2O = SO42-+2Fe2++4H+ �ۢܢݢ� ͨ��N2�ų�װ���е�SO2����ֹ������Ⱦ��
CuSO4+ SO2��+ 2H2O ��� ���ɻ�ɫ���� SO2+2H2S=S��+ 2H2O ��ˮ��ɫ SO2+Cl2+ 2H2O =2HCl+ H2SO4 �������ᱵ�İ�ɫ���� SO2+H2O2+BaCl2= BaSO4��+2HCl SO2+2Fe3++2H2O = SO42-+2Fe2++4H+ �ۢܢݢ� ͨ��N2�ų�װ���е�SO2����ֹ������Ⱦ��
��������
Cu��Ũ�����ڼ��������·�Ӧ������SO2��SO2Ϊ�����������ʹ��ɫʯ����Һ��죻SO2����Ϊ�����ԣ����������ᷴӦ�����ɻ�ɫ������SO2����Ϊ��ԭ�ԣ��������������ʷ�Ӧ��SO2�Ի����к���ʵ��ʱҪ��NaOH����β��������
(1) Cu��Ũ�����ڼ��������·�ӦΪ��Cu+2H2SO4![]() CuSO4+ SO2��+2 H2O���ʴ�Ϊ��Cu+2H2SO4
CuSO4+ SO2��+2 H2O���ʴ�Ϊ��Cu+2H2SO4![]() CuSO4+ SO2��+ 2H2O��
CuSO4+ SO2��+ 2H2O��
(2)��SO2Ϊ�����������ʹ��ɫʯ����Һ��죬�ʴ�Ϊ����죻
����Ϊ��������Һ��SO2����Ϊ�����ԣ����������ᷴӦ�����ɻ�ɫ��������ӦΪSO2+2H2S=S��+ 2H2O���ʴ�Ϊ�����ɻ�ɫ������SO2+2H2S=S��+ 2H2O��
����Ϊ��ˮ��SO2����Ϊ��ԭ�ԣ���ʹ��ˮ��ɫ����ӦΪSO2+Cl2+ 2H2O =2HCl+ H2SO4���ʴ�Ϊ����ˮ��ɫ��SO2+Cl2+ 2H2O =2HCl+ H2SO4��
����Ϊ˫��ˮ���Ȼ�����H2O2��SO2����Ϊ�������������뱵���ӽ�ϣ��������ᱵ�İ�ɫ��������ӦΪSO2+H2O2+BaCl2= BaSO4��+2HCl���ʴ�Ϊ���������ᱵ�İ�ɫ������SO2+H2O2+BaCl2= BaSO4��+2HCl��
����Ϊ�Ȼ�����Һ��ͨ�����������Һ�ɻ�ɫ��Ϊdz��ɫ�������Ȼ��������ԣ����ӷ���ʽΪSO2+2Fe3++2H2O = SO42-+2Fe2++4H+���ʴ�Ϊ��SO2+2Fe3++2H2O = SO42-+2Fe2++4H+��
(3)�ۢܢݢ���װ�еĶ���ǿ���������ʣ�����SO2����������ԭ��Ӧ����SO2Ϊ��ԭ�����ʴ�Ϊ���ۢܢݢ���
(4) SO2�Ի����к���ʵ��ʱҪ��NaOH�����ɾ����ʴ�Ϊ��ͨ��N2�ų�װ���е�SO2����ֹ������Ⱦ��

 �����ҵ���������ϵ�д�
�����ҵ���������ϵ�д� �����̸�Ӯ����ٸ�Ч�����ܸ�ϰ���ϿƼ�������ϵ�д�
�����̸�Ӯ����ٸ�Ч�����ܸ�ϰ���ϿƼ�������ϵ�д� �����ҵ�����������ѧ���ӳ�����ϵ�д�
�����ҵ�����������ѧ���ӳ�����ϵ�д�