题目内容
(1)配制100 mL 0.10 mol·L-1NaOH标准溶液。
①主要操作步骤:计算→称量→溶解→___ ___(冷却后)→洗涤(并将洗涤液移入容量瓶)→___ ___→___ ___→将配制好的溶液倒入试剂瓶中,贴上标签。
②称量________g氢氧化钠固体所需仪器有:托盘天平(带砝码、镊子)、________、________。
(2)取20.00 mL待测盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用已配制的NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
实验 | NaOH溶液的浓度(mol·L-1) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸的体积(mL) |
1 | 0.10 | 22.62 | 20.00 |
2 | 0.10 | 22.72 | 20.00 |
3 | 0.10 | 22.80 | 20.00 |
①滴定达到终点的标志是___________________________________________________________________。
②根据上述数据,可计算出该盐酸的浓度约为_____________(保留两位有效数字)。
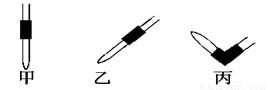
③排去碱式滴定管中气泡的方法应采用如图所示操作中的________,然后轻轻挤压玻璃球使尖嘴部分充满碱液。
④在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有________(填字母序号)。
A.滴定终点读数时俯视
B.酸式滴定管使用前,水洗后未用待测盐酸润洗
C.锥形瓶水洗后未干燥
D.称量NaOH固体中混有Na2CO3固体
E.碱式滴定管尖嘴部分有气泡,滴定后消失
练习册系列答案
相关题目
下列生活中常见的现象中,其反应原理不涉及氧化还原反应的是
A.铁的冶炼 | B.电池放电 | C.碳酸氢钠作发酵粉 | D.天然气燃烧 |
|
|
|
|








 .2 L
.2 L .25℃,1.01×105Pa,64 g SO2中含有的原子数为3NA
.25℃,1.01×105Pa,64 g SO2中含有的原子数为3NA CO(g)+Cl2(g) ΔH >0,当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,其中能提高 COCl2转化率的是
CO(g)+Cl2(g) ΔH >0,当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,其中能提高 COCl2转化率的是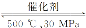 2NH3(g) ΔH=-38.6 kJ·mol-1
2NH3(g) ΔH=-38.6 kJ·mol-1 O2(g)===H2O(g) ΔH=-242 kJ·mol-1
O2(g)===H2O(g) ΔH=-242 kJ·mol-1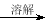
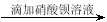 白色沉淀
白色沉淀 沉淀不溶解→说明试样已变质
沉淀不溶解→说明试样已变质
 精盐
精盐 溶液颜色无变化
溶液颜色无变化 溶液变红色→溶液中含有Fe2+
溶液变红色→溶液中含有Fe2+
 溶液变紫色→氧化性:H2O2>I2
溶液变紫色→氧化性:H2O2>I2