题目内容
3.(1)常温下0.1mol•L-1CH3COONa溶液呈碱(选填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):CH3COO-+H2O=CH3COOH+OH-.(2)在配制碳酸钠溶液时,为了防止发生水解,可以加入少量的NaOH(或NaHCO3).(填化学式)
(3)写出泡沫灭火器(内含NaHCO3溶液和Al2(SO4)3溶液)倒置时反应的离子方程式为Al3++3HCO3-=Al(OH)3↓+3CO2↑.
(4)常温下,0.1mol•L-1NaHCO3溶液的pH大于8,则溶液中c(H2CO3)>c(CO32-)(填“>”、“=”或“<”),原因是HCO3-?CO32-+H+、HCO3-+H20?H2CO3+OH-,HCO3-的水解程度大于电离程度(用离子方程式和必要的文字说明).
(5)已知:
①ZnCl2•xH2O易溶于水,且其水溶液呈酸性
②SOCl2极易与水发生下列反应:SOCl2+H2O═SO2+2HCl
实验室制取无水氯化锌是将ZnCl2•xH2O与SOCl2混合加热的方法.
请回答下列问题:
混合加热时发生的化学方程式:ZnCl2•XH2O+XSOCl2$\frac{\underline{\;\;△\;\;}}{\;}$ZnCl2+XSO2+2XHCl;SOCl2的作用是夺取ZnCl2•XH2O中的结晶水,生成的HCl抑制ZnCl2•XH2O的水解.
分析 (1)0.1mol•L-1CH3COONa溶液中醋酸根离子水解溶液显碱性,醋酸根离子水解生成醋酸和氢氧根离子;
(2)碳酸钠为强碱弱酸盐,在溶液中存在水解平衡,从平衡移动的角度分析并解答该题;
(3)NaHCO3与Al2(SO4)3发生相互促进的水解反应生成二氧化碳和氢氧化铝;
(4)0.1mol•L-1NaHCO3溶液的pH大于8,说明碳酸氢根离子的水解程度大于电离程度;
(5)ZnCl2•xH2O易溶于水,且其水溶液呈酸性,氯化锌水解生成氢氧化锌和盐酸,溶液显酸性,SOCl2极易与水发生生成二氧化硫和盐酸,其中盐酸起到抑制氯化锌的水解,晶体和SOCl2混合加热,结晶水失去和SOCl2极易和水反应生成盐酸和二氧化硫.
解答 解:(1)0.1mol•L-1CH3COONa溶液中醋酸根离子水解溶液显碱性,醋酸根离子水解生成醋酸和氢氧根离子,反应的离子方程式:CH3COO-+H2O=CH3COOH+OH-,
故答案为:碱,CH3COO-+H2O=CH3COOH+OH-;
(2)碳酸钠为强碱弱酸盐,在溶液中存在水解平衡:CO32-+H2O?HCO3-+OH-,为了防止发生水解,可以加入少量NaOH或NaHCO3,使平衡向逆反应方向移动,从而抑制水解,
故答案为:NaOH (或NaHCO3);
(3)NaHCO3与Al2(SO4)3发生相互促进的水解反应生成二氧化碳和氢氧化铝,其反应的离子方程式为:Al3++3HCO3-=Al(OH)3↓+3CO2↑;
故答案为:Al3++3HCO3-=Al(OH)3↓+3CO2↑;
(4)常温下,0.1mol•L-1NaHCO3溶液中存在电离和水解,离子方程式为:HCO3-?CO32-+H+、HCO3-+H20?H2CO3+OH-,的pH大于8,c(OH-)>c(H+),说明HCO3-水解程度大于其电离程度,故c(Na+)>c(HCO3-)、c(H2CO3)>c(CO32-),
故答案为:>;HCO3-?CO32-+H+、HCO3-+H20?H2CO3+OH-,HCO3-的水解程度大于电离程度;
(5)ZnCl2•xH2O易溶于水,且其水溶液呈酸性,氯化锌水解生成氢氧化锌和盐酸,溶液显酸性,SOCl2极易与水发生生成二氧化硫和盐酸,其中盐酸起到抑制氯化锌的水解,晶体和SOCl2混合加热,反应的化学方程式为:ZnCl2•XH2O+XSOCl2 $\frac{\underline{\;\;△\;\;}}{\;}$ZnCl2+XSO2+2XHCl,结晶水失去和SOCl2极易和水反应生成盐酸和二氧化硫,
SOCl2的作用是夺取ZnCl2•XH2O中的结晶水,生成的HCl抑制ZnCl2•XH2O的水解,
故答案为:ZnCl2•XH2O+XSOCl2 $\frac{\underline{\;\;△\;\;}}{\;}$ZnCl2+XSO2+2XHCl;夺取ZnCl2•XH2O中的结晶水,生成的HCl抑制ZnCl2•XH2O的水解.
点评 本题考查了盐类水解的原理分析判断,溶液酸碱性比较,弱离子的性质应用,掌握基础是解题关键,题目难度中等.

 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案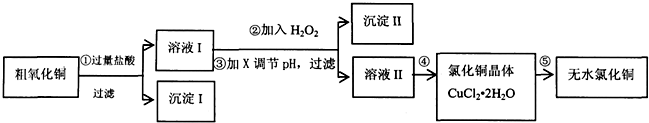
(1)步骤①中氧化铜与盐酸反应的离子方程式:CuO+2H+=Cu2++H2O.
(2)步骤②中加入H2O2的目的:将Fe2+氧化成Fe3+,沉淀Ⅱ的化学式为:Fe(OH)3.
(3)已知:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
| Fe2+ | 7 | 9 |
A.NaOH B.CuO C.Cu(OH)2 D.NH3•H2O
(4)步骤④的操作是蒸发浓缩、冷却结晶,过滤、洗涤、干燥.为得到无水CuCl2,步骤⑤需在干燥的HCl气流中加热CuCl2•2H2O,原因是干燥的HCl气流既可抑制Cu2+的水解,还能带走CuCl2•2H2O受热产生的水汽.
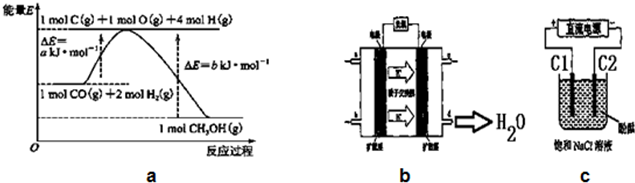
(1)写出合成甲醇的热化学方程式CO(g)+2H2(g)=CH3OH(g)△H=-(b-a)KJ/mol.
(2)实验室在1L的密闭容器中进行模拟合成实验.将1mol CO和2mol H2通入容器中,分别恒温在300℃和500℃反应,每隔一段时间测得容器内CH3OH的浓度如下表所示:
| 时间浓度(mol/L)温度 | 10min | 20min | 30min | 40min | 50min | 60min |
| 300℃ | 0.40 | 0.60 | 0.75 | 0.84 | 0.90 | 0.90 |
| 500℃ | 0.60 | 0.75 | 0.78 | 0.80 | 0.80 | 0.80 |
(3)在500℃达到平衡时,平衡常数K=25.
(4)在另一体积不变的密闭容器中,充入1.2mol CO和2.0mol H2,一定条件下达到平衡,测得容器中压强为起始压强的一半.计算该条件下H2的转化率为80%.
(5)铜基催化剂具有活性高、选择性好和条件温和的特点,已广泛地使用于CO/CO2的加氢合成甲醇.使用铜基催化剂后,该反应中a的大小变化对反应热△H有无影响,无影响.(填“有影响”或“无影响”)
(6)2009年,长春应用化学研究所在甲醇燃料电池技术上获得新突破,原理如图b所示.请写出从C口通入O2发生的电极反应式O2+4e-+4H+=2H2O.
(7)用上述电池做电源,用图c装置电解饱和食盐水(C1、C2均为石墨电极).
①该反应的离子方程式2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑.
②电解开始后在电极C2的周围(填“C1”或“C2”)先出现红色.

实验药品:铜,铁,镁,0.5mol/L H2SO4,2mol/L H2SO4,18.4mol/L H2SO4
Ⅰ.甲同学研究的实验报告如表:
| 实验步骤 | 现象 | 结论 |
| ①分别取等体积的 2 mol/L的硫酸于试管 | 反应速率:镁>铁,铜不反应 | 金属的性质越活泼,反应速率越快 |
(1)甲同学表中实验步骤②为分别投入大小、形状相同的Cu、Fe、Mg.
(2)甲同学的实验目的是探究反应物本身的性质对反应速率的影响;要得出正确的实验结论,还需控制的实验条件是温度相同.
Ⅱ.乙同学为了更精确的研究浓度对反应速率的影响,利用右图所示装置进行实验,
(3)乙同学在实验中应该测定的数据是一定时间内产生气体的体积(或产生一定体积的气体所需的时间).
(4)乙同学完成该实验应选用的实验药品镁(或铁)和0.5mol/LH2SO4、2mol/LH2SO4.
(5)图中仪器A的名称是分液漏斗,检验该装置气密性的方法是按住注射器活塞不动,向分液漏斗中倒水,液面高度不变,说明装置气密性良好.