题目内容
【题目】25℃时,向1L c(HA)+c(A-)=0.1mol/L的溶液中滴加盐酸或NaOH溶液,溶液中的H+、OH-、A-及HA的浓度的对数值(lgc)与pH的关系如图所示(不考虑溶液温度变化),下列说法正确的是
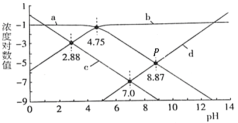
A.a表示lgc(A-)与pH的关系曲线
B.K(HA)的数量级为10-5
C.P点溶液中n(Na+)+ n(H+)=0.1mol
D.滴加盐酸或NaOH溶液的过程中c(HA)·c(OH-)均增大
【答案】BC
【解析】
根据图像分析,微粒浓度的对数越大离子浓度越大,随着pH的增大,溶液碱性增强,酸性减弱,则氢离子浓度逐渐减小,氢氧根离子浓度逐渐增大;c的浓度对数值在减小,为c(H+)浓度变化曲线;d的浓度对数值在增大,为c(OH-)浓度变化曲线;pH小于4.75时,a的浓度对数值不变,pH越大,a的浓度对数值减小,应该是c(HA)的变化曲线;b的浓度对数值随pH的增大而增大,b为c(A-)变化曲线;
A. 根据上述分析a表示lg c(HA)与pH的关系曲线,故A错误;
B.K(HA)的表达式为K(HA)= ,pH=4.75时,c(HA)=c(A-),K(HA)=
,pH=4.75时,c(HA)=c(A-),K(HA)= =10-4.75≈1.78×10-5,数量级为10-5,故B正确;
=10-4.75≈1.78×10-5,数量级为10-5,故B正确;
C.P点时,c(OH-)=c(HA),P点的电荷守恒式为c(H+)+ c(Na+)= c(A-) +c(OH-),变式为 c(H+)+ c(Na+)=c(A-)+c(HA),根据题中信息,1Lc(HA)+c(A-)=0.1mol/L的溶液中,n(HA)+n(A-)=0.1mol/L×1L=0.1mol,则溶液中n(Na+)+ n(H+)=0.1mol,故C正确;
D. 滴加盐酸或NaOH溶液的过程中,K(HA)=  ,c(H+)=
,c(H+)= , K(HA)=
, K(HA)= ,K(HA)、Kw只受温度影响,温度不变,平衡常数不变,滴加盐酸,c(A-)在减小,c(OH-)c(HA)在减小,故D错误;
,K(HA)、Kw只受温度影响,温度不变,平衡常数不变,滴加盐酸,c(A-)在减小,c(OH-)c(HA)在减小,故D错误;
答案选BC。

【题目】今有氧、镁、铝、硫、铬5种元素,试回答下列问题
(1)镁晶体堆积方式为___堆积(选填:“简单立方”、“体心立方”、“面心立方”、“六方”);
(2)用“>”、“<”填写下表
第一电离能 | 电负性 | 晶格能 | 沸点 |
Mg___Al | O___S | MgO___MgS | H2O___H2S |
(3)基态铬原子外围电子轨道表示式为___。
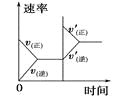
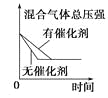
【题目】对于可逆反应N2(g)+3H2(g) ![]() 2NH3(g) △H<0,下列研究目的和示意图相符的是( )
2NH3(g) △H<0,下列研究目的和示意图相符的是( )
A | B | C | D | |
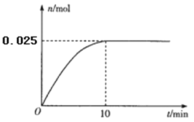
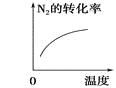
研究目的 | 压强对反应的影响 (p2>p1) | 温度对反应的影响 | 平衡体系中增加N2的浓度对反应的影响 | 催化剂对反应的影响 |
示意图 |
|
|
|
|
A.AB.BC.CD.D