题目内容
下列有关物质结构和性质的说法中,正确的是( )
| A.因为水溶液的酸性:HCl>H2S,所以非金属性:Cl>S |
| B.同周期第ⅡA族与第IIIA族的元素原子序数之差不一定为1 |
| C.元素原子的最外层电子数越多,越容易得电子,非金属性越强 |
| D.同周期主族元素的原子形成的简单离子电子层结构相同 |
B
解析试题分析:A、根据最高价氧化物水合物的酸性强弱比较非金属性,错误;B、第4、5、6、7周期同周期第ⅡA族与第IIIA族之间出现了过渡元素,正确;C、非金属性强弱与元素原子的最外层电子数的多少无关,错误;D、同周期主族元素金属与非金属原子形成的简单电子层结构不同,错误。
考点:本题考查原子结构、元素周期表、非金属性强弱的判断。

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案
相关题目
有一合金由X、Y、Z、W四种金属组成,①若将合金放入盐酸中只有Z、Y能溶解;②若将合金于潮湿空气中,表面只出现Z的化合物;③若将该合金作阳极,用X盐溶液作电解质溶液,通电时四种金属都以离子形式进入溶液中,在阴极上只析出X。这四种金属活动性顺序是
| A.Y>Z>W>X | B.Z>Y>W>X |
| C.W>Z>Y>X | D.X>Y>Z>W |
若M是ⅡA族的某元素,则与M同周期且相邻的元素不可能位于元素周期表的
| A.ⅠA | B.ⅠB | C.ⅢA | D.ⅢB |
短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4︰3,Z原子比X原子的核外电子数多4。下列说法正确的是 ( )
| A.W、Y、Z的氢化物稳定性顺序可能是W>Z>Y |
| B.W、X、Y、Z的原子半径大小顺序Z<Y<X<W |
| C.Z的氧化物对应水化物的酸性一定强于W氧化物对应水化物的酸性 |
| D.Z的某种氧化物可以做新型消毒剂 |
下列顺序不正确的是
| A.热稳定性:HF > HCl > HBr > HI |
| B.微粒的半径:Cl-> Na+> Mg2+> Al3+ |
| C.电离程度(同温度同浓度溶液中):HCl > CH3COOH > NaHCO3 |
| D.分散质粒子的直径:Fe(OH)3悬浊液 > Fe(OH)3胶体 > FeCl3溶液 |
短周期主族元素X、Y、Z、W、Q的原子序数依次增大,X的气态氢化物极易溶于Y的氢化物中,常温下,Z的单质能溶于W的最高价氧化物的水化物的稀溶液,却不溶于其浓溶液。下列说法正确的是
| A.元素Y的最高正化合价为+6 |
| B.离子半径的大小顺序为W>Q>Z>X>Y |
| C.氢化物的沸点Y>W |
| D.元素W的最高价氧化物对应水化物的酸性比Q的强 |
元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中Z的一种氧化物能使品红溶液褪色,则下列说法正确的是( )
| A.非金属性:R<T<Q | B.T与Q的电子数相差18 |
| C.原子半径:R< T< Z | D.X的氧化物既能与盐酸反应又能与氢氧化钠溶液反应 |
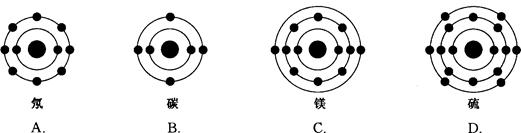
 下列原子中,与氧元素原子的化学性质相似的是( )
下列原子中,与氧元素原子的化学性质相似的是( )