题目内容
已知:核电荷数小于18的三种元素X、Y、Z;X原子最外能层的p能级中有一个轨道填充了2个电子,Y原子的最外层中p能级的电子数等于前一能层电子总数,且X和Y具有相同的电子层;Z与X在周期表中位于同一主族.回答下列问题:
(1)X的价电子排布式为 ,Y的轨道表示式为 .
(2)ZX2的分子构型为 ,YX2的电子式为 .
(3)Y与Z形成的化合物中化学键是 键(填“极性”或“非极性”,下同),该分子属于 分子.
(4)X的最简单氢化物中键角为 ,Y的最简单氢化物中中心原子是 杂化.
(1)X的价电子排布式为
(2)ZX2的分子构型为
(3)Y与Z形成的化合物中化学键是
(4)X的最简单氢化物中键角为
分析:核电荷数小于18的三种元素X、Y、Z,X原子最外能层的p能级中有一个轨道填充了2个电子,则X位于最外层电子排布式为ns2np4,为第VIA族元素;
Y原子的最外层中p能级的电子数等于前一能层电子总数,p能级最多排列6个电子,则Y次外层为K层,Y原子最外层p能级上电子数是2,Y原子含有6个电子,为C元素,且X和Y具有相同的电子层,即二者为同一周期元素,所以X是O元素,Z与X在周期表中位于同一主族,且X和Z原子序数都小于18,所以Z为S元素,结合元素、物质的结构来分析解答.
Y原子的最外层中p能级的电子数等于前一能层电子总数,p能级最多排列6个电子,则Y次外层为K层,Y原子最外层p能级上电子数是2,Y原子含有6个电子,为C元素,且X和Y具有相同的电子层,即二者为同一周期元素,所以X是O元素,Z与X在周期表中位于同一主族,且X和Z原子序数都小于18,所以Z为S元素,结合元素、物质的结构来分析解答.
解答:解:核电荷数小于18的三种元素X、Y、Z,X原子最外能层的p能级中有一个轨道填充了2个电子,则X位于最外层电子排布式为ns2np4,为第VIA族元素;
Y原子的最外层中p能级的电子数等于前一能层电子总数,p能级最多排列6个电子,则Y次外层为K层,Y原子最外层p能级上电子数是2,Y原子含有6个电子,为C元素,且X和Y具有相同的电子层,即二者为同一周期元素,所以X是O元素,Z与X在周期表中位于同一主族,且X和Z原子序数都小于18,所以Z为S元素,
(1)X是O元素,其最外层有6个电子,主族元素的最外层电子就是其价电子,所以X价电子排布式为2s22p4,
Y是C原子,根据构造原理知,其核外电子排布式为:1s22s22p2,所以其轨道表示式为 ,
,
故答案为:1s22s22p2; ;
;
(2)SO2的分子中价层电子对个数是2+
(6-2×2)=3,且含有一个孤电子对,所以其空间构型为V型,CO2为共价化合物,其电子式为 ,故答案为:V型;
,故答案为:V型; ;
;
(3)C与S形成的化合物是二硫化碳,二硫化碳中碳原子和硫原子之间存在极性键,但二硫化碳分子中正负电荷重心重合,为非极性分子,故答案为:极性;非极性;
(4)O的最简单氢化物是水,水分子是V形结构,水分子中中键角为104.5°,C的最简单氢化物是甲烷,甲烷分子中碳原子含有4个共价单键,且不含孤电子对,所以碳原子为sp3杂化,
故答案为:104.5°;sp3.
Y原子的最外层中p能级的电子数等于前一能层电子总数,p能级最多排列6个电子,则Y次外层为K层,Y原子最外层p能级上电子数是2,Y原子含有6个电子,为C元素,且X和Y具有相同的电子层,即二者为同一周期元素,所以X是O元素,Z与X在周期表中位于同一主族,且X和Z原子序数都小于18,所以Z为S元素,
(1)X是O元素,其最外层有6个电子,主族元素的最外层电子就是其价电子,所以X价电子排布式为2s22p4,
Y是C原子,根据构造原理知,其核外电子排布式为:1s22s22p2,所以其轨道表示式为
 ,
,故答案为:1s22s22p2;
 ;
;(2)SO2的分子中价层电子对个数是2+
| 1 |
| 2 |
 ,故答案为:V型;
,故答案为:V型; ;
;(3)C与S形成的化合物是二硫化碳,二硫化碳中碳原子和硫原子之间存在极性键,但二硫化碳分子中正负电荷重心重合,为非极性分子,故答案为:极性;非极性;
(4)O的最简单氢化物是水,水分子是V形结构,水分子中中键角为104.5°,C的最简单氢化物是甲烷,甲烷分子中碳原子含有4个共价单键,且不含孤电子对,所以碳原子为sp3杂化,
故答案为:104.5°;sp3.
点评:本题考查了元素位置、结构和性质相互关系的应用,涉及杂化方式的判断、电子式的书写、分子空间构型的判断等知识点,根据电子排布正确推断元素是解本题关键,结合价层电子对互斥理论来分析解答,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
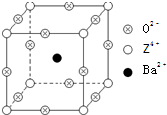 (2011?江西二模)已知X、Y和Z三种元素的原子序数之和等于48.X的一种1:1型氢化物分子中既有σ键又有π键.Z是金属元素,Z的单质和化合物有广泛的用途.已知Z的核电荷数小于28,且次外层有2个未成对电子.工业上利用ZO2和碳酸钡在熔融状态下制取化合物M(M可看做一种含氧酸盐).M有显著的“压电性能”,应用于超声波的发生装置.经X射线分析,M晶体的最小重复单位为正方体(如图),边长为4.03×10-10m,顶点位置为Z4+所占,体心位置为Ba2+所占,所有棱心位置为O2-所占.
(2011?江西二模)已知X、Y和Z三种元素的原子序数之和等于48.X的一种1:1型氢化物分子中既有σ键又有π键.Z是金属元素,Z的单质和化合物有广泛的用途.已知Z的核电荷数小于28,且次外层有2个未成对电子.工业上利用ZO2和碳酸钡在熔融状态下制取化合物M(M可看做一种含氧酸盐).M有显著的“压电性能”,应用于超声波的发生装置.经X射线分析,M晶体的最小重复单位为正方体(如图),边长为4.03×10-10m,顶点位置为Z4+所占,体心位置为Ba2+所占,所有棱心位置为O2-所占.