题目内容
7.常温下,下列各组离子在指定溶液中一定能大量共存的是( )| A. | 无色溶液中:Cr2O${\;}_{7}^{2-}$、Fe3+、SCN-、Cl- | |
| B. | 能使石蕊呈蓝色的溶液中:Na+、K+、NO${\;}_{3}^{-}$、CO${\;}_{3}^{2-}$ | |
| C. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012 的溶液中:S2O${\;}_{3}^{2-}$、CrO${\;}_{4}^{2-}$、Cl-、Mg2+ | |
| D. | 水电离的c (H)=10-12mol•L-1 的溶液中:HCO${\;}_{3}^{-}$、SiO${\;}_{3}^{2-}$、Cu2+、NH${\;}_{4}^{+}$ |
分析 A.离子之间结合生成络离子,且含有色离子;
B.能使石蕊呈蓝色的溶液,显碱性;
C.$\frac{c({H}^{+})}{c(O{H}^{-})}$=1012 的溶液,显酸性;
D.水电离的c (H)=10-12mol•L-1 的溶液,为酸或碱溶液.
解答 解:A.Fe3+、SCN-结合生成络离子,且Fe3+、Cr2O72-均为有色离子,故A错误;
B.能使石蕊呈蓝色的溶液,显碱性,该组离子之间不反应,可大量共存,故B正确;
C.$\frac{c({H}^{+})}{c(O{H}^{-})}$=1012 的溶液,显酸性,酸性溶液中不能存在S2O32-、CrO42-,故C错误;
D.水电离的c (H)=10-12mol•L-1 的溶液,为酸或碱溶液,酸溶液中不能大量存在HCO3-、SiO32-,碱溶液中不能大量存在HCO3-、NH4+,故D错误;
故选B.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
17.下列过程属于熵增加的是( )
| A. | 一定条件下水由气态变为液态 | B. | 水总是由高处流向低处 | ||
| C. | 碳酸氢铵在常温情况下分解 | D. | CO点燃时生成CO2 |
18.已知Co2O3在酸性溶液中易被还原成Co2+;且Co2O3、Cl2、FeCl3、I2的氧化性依次减弱.下列反应在水溶液中不可能发生的是( )
| A. | Cl2通入FeI2溶液中,可存在反应3Cl2+6FeI2=2FeCl3+4FeI3 | |
| B. | 每1mol Co2O3在酸性溶液中被还原生成Co2+时转移2 mol e- | |
| C. | FeCl3溶液能使淀粉-KI试纸变蓝 | |
| D. | I2具有较弱的氧化性,不可以将Co2+氧化成Co2O3 |
2.下列变化克服的作用力完全相同的是( )
| A. | 碘和干冰的升华 | |
| B. | 分别将NaHSO4熔化、溶解于水 | |
| C. | HCl和MgCl2的溶解 | |
| D. | 常压下分别将NaHCO3高温加热、溶解于水 |
12.下列事实中,不能用平衡移动原理解释的是( )
| A. | 开启啤酒瓶后,瓶中马上泛起大量泡沫 | |
| B. | 对CO(g)+NO2(g)═CO2(g)+NO(g)平衡体系增大压强可使其颜色变深 | |
| C. | 常温下,将1mLpH=3的醋酸溶液加水稀释到100mL,测得其pH<5 | |
| D. | 实验室中常用排饱和食盐水的方法收集氯气 |
19.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | Kw/c(H+)=1 mol•L-1的溶液中:Na+、SiO32-、I-、CO32- | |
| B. | 氨水中:Al3+、K+、F-、NO3- | |
| C. | pH=1的溶液中:NH4+、Na+、SO42-、CH3COO- | |
| D. | 0.1 mol•L-1的NaHSO4溶液中:K+、Fe2+、Cl-、NO3- |
16.天津港爆炸现场的氰化钠有剧毒,用过氧化氢处理含氰废水的第一步反应原理如下:CN-+H2O2$\frac{\underline{\;催化剂\;}}{\;}$CNO-+H2O.下列说法正确的是( )
| A. | 反应中H2O2被氧化 | |
| B. | CNO-中N的化合价为-3价 | |
| C. | 温度越高越有利于该反应发生 | |
| D. | 每生成1.8 g H2O,转移电子数为0.4NA |
 .
. .
. .
.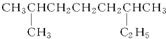 系统命名:2,6二甲基辛烷;
系统命名:2,6二甲基辛烷; ;
; ;②乙醛与银氨溶液水浴加热CH3CHO+2Ag(NH3)2OH$\stackrel{△}{→}$CH3COONH4+2Ag+3NH3+H2O;
;②乙醛与银氨溶液水浴加热CH3CHO+2Ag(NH3)2OH$\stackrel{△}{→}$CH3COONH4+2Ag+3NH3+H2O;