题目内容
 NH4Al(SO4)2是加工食品最为快捷的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业有广泛应用.试回答下列问题:
NH4Al(SO4)2是加工食品最为快捷的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业有广泛应用.试回答下列问题:(1)NH4Al(SO4)2可用做净水剂,其理由是
(2)相同条件下,浓度相同的NH4Al(SO4)2溶液和NH4HSO4溶液中,NH4+浓度较大的是
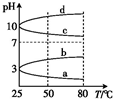
(3)如图是0.1mol?L-1某电解质溶液的pH随温度变化的图象.其中符合0.1mol?L-1NH4Al(SO4)2溶液的pH随温度变化的曲线是
(4)室温时,向100mL 0.1mol?L-1NH4HSO4溶液中滴加0.1mol?L-1NaOH溶液,NH4HSO4溶液中首先与OH-发生反应的离子是
考点:镁、铝的重要化合物,酸碱混合时的定性判断及有关ph的计算
专题:
分析:(1)Al3+水解生成的Al(OH)3具有吸附性;
(2)NH4Al(SO4)2中Al3+水解呈酸性抑制NH4+水解,HSO4-电离出H+同样抑制NH4+水解;
(3)NH4Al(SO4)2水解,溶液呈酸性,升高温度其水解程度增大;
(4)向100mL 0.1mol?L-1NH4HSO4溶液中滴加0.1mol?L-1NaOH溶液,NH4HSO4溶液电离生成铵根、氢离子和硫酸根,所以首先与OH-发生反应的离子是H+,当pH=7时根据电荷守恒判断.
(2)NH4Al(SO4)2中Al3+水解呈酸性抑制NH4+水解,HSO4-电离出H+同样抑制NH4+水解;
(3)NH4Al(SO4)2水解,溶液呈酸性,升高温度其水解程度增大;
(4)向100mL 0.1mol?L-1NH4HSO4溶液中滴加0.1mol?L-1NaOH溶液,NH4HSO4溶液电离生成铵根、氢离子和硫酸根,所以首先与OH-发生反应的离子是H+,当pH=7时根据电荷守恒判断.
解答:
解:(1)Al3+水解生成的Al(OH)3具有吸附性,离子方程式:Al3++3H2O═Al(OH)3+3H+,Al(OH)3吸附悬浮颗粒使其沉降从而净化水,
故答案为:Al3+水解生成的Al(OH)3具有吸附性,即Al3++3H2O═Al(OH)3+3H+,Al(OH)3吸附悬浮颗粒使其沉降从而净化水;
(2)NH4Al(SO4)2与NH4HSO4中的NH4+均发生水解,但是NH4Al(SO4)2中Al3+水解呈酸性抑制NH4+水解,HSO4-电离出H+同样抑制NH4+水解,因为HSO4-电离生成的H+浓度比Al3+水解生成的H+浓度大,所以NH4HSO4中NH4+水解程度比NH4Al(SO4)2中的小,则NH4+浓度较大的是NH4HSO4溶液,故答案为:NH4HSO4溶液;
(3)NH4Al(SO4)2水解,溶液呈酸性,升高温度其水解程度增大,pH减小,符合的曲线为a,
故答案为:a;NH4Al(SO4)2水解,溶液呈酸性,升高温度,其水解程度增大,pH减小;
(4)向100mL 0.1mol?L-1NH4HSO4溶液中滴加0.1mol?L-1NaOH溶液,NH4HSO4溶液电离生成铵根、氢离子和硫酸根,所以首先与OH-发生反应的离子是H+,当pH=7时,则根据电荷守恒c(NH4+)+c(Na+)+c(H+)=2c(SO42-)+c(OH-),所以c(NH4+)+c(Na+)=2c(SO42-),故答案为:H+;=.
故答案为:Al3+水解生成的Al(OH)3具有吸附性,即Al3++3H2O═Al(OH)3+3H+,Al(OH)3吸附悬浮颗粒使其沉降从而净化水;
(2)NH4Al(SO4)2与NH4HSO4中的NH4+均发生水解,但是NH4Al(SO4)2中Al3+水解呈酸性抑制NH4+水解,HSO4-电离出H+同样抑制NH4+水解,因为HSO4-电离生成的H+浓度比Al3+水解生成的H+浓度大,所以NH4HSO4中NH4+水解程度比NH4Al(SO4)2中的小,则NH4+浓度较大的是NH4HSO4溶液,故答案为:NH4HSO4溶液;
(3)NH4Al(SO4)2水解,溶液呈酸性,升高温度其水解程度增大,pH减小,符合的曲线为a,
故答案为:a;NH4Al(SO4)2水解,溶液呈酸性,升高温度,其水解程度增大,pH减小;
(4)向100mL 0.1mol?L-1NH4HSO4溶液中滴加0.1mol?L-1NaOH溶液,NH4HSO4溶液电离生成铵根、氢离子和硫酸根,所以首先与OH-发生反应的离子是H+,当pH=7时,则根据电荷守恒c(NH4+)+c(Na+)+c(H+)=2c(SO42-)+c(OH-),所以c(NH4+)+c(Na+)=2c(SO42-),故答案为:H+;=.
点评:本题考查盐类的水解和离子浓度大小的比较,题目难度较大,注意电解质溶液中离子浓度大小和电荷守恒守恒的分析应用.

练习册系列答案
相关题目
某溶液中含有下列离子中的若干种,K+、Cu2+、Al3+、Fe2+、Cl-、CO32-、NO3-、SO42-,且各种离子的物质的量浓度相等.现取三份溶液进行如下实验:
①第一份溶液:加入BaCl2溶液,有白色沉淀生成.
②第二份溶液:用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃观察,没有紫色火焰.
③第三份溶液:加入足量稀盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液中阴离子种类不变.根据上述实验,以下推测正确的是( )
①第一份溶液:加入BaCl2溶液,有白色沉淀生成.
②第二份溶液:用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃观察,没有紫色火焰.
③第三份溶液:加入足量稀盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液中阴离子种类不变.根据上述实验,以下推测正确的是( )
| A、步骤①中的白色沉淀为2种钡盐 |
| B、溶液中难以确定Cl-的存在与否 |
| C、原溶液中所含的离子有5种 |
| D、步骤③中可以确定Fe2+、NO3-的存在,不能确定其它离子是否存在 |
用铁酸钠(Na2FeO4)对河湖的淡水消毒是城市饮用水处理新技术,下列对Na2FeO4用于饮用水消毒处理的分析正确的是( )
| A、Na2FeO4在溶液中显强酸性,能消毒杀菌 |
| B、在Na2FeO4中Fe为+6价,具有强氧化性,能消毒杀菌 |
| C、Na2FeO4的还原产物Fe3+易水解为Fe(OH)3胶体,可使水中悬浮物凝聚沉降 |
| D、Na2FeO4的还原产物Fe2+易水解为Fe(OH)2胶体,可使水中悬浮物凝聚沉降 |
化学物A的结构简式是HO-CH2-CBr2-O-CBr2-CH2-OH,下列有关A的叙述正确的是( )
| A、不能发生消去反应 |
| B、能发生取代反应 |
| C、能溶于水 |
| D、不能氧化为醛 |
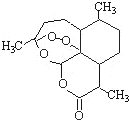 被誉为中国“新四大发明”的复方蒿甲醚是第一个由中国发现的全新化学结构的药品,也是目前在国际上获得广泛认可的中国原创药品.至今已被多个亚非国家指定为疟疾治疗一线用药,它在疟疾这一高传染性疾病治疗史上具有里程碑意义.其主要成分是青蒿素(是一种由青蒿中分离得到的具有新型化学结构的抗疟药),结构如图所示.有关该化合物的叙述正确的是( )
被誉为中国“新四大发明”的复方蒿甲醚是第一个由中国发现的全新化学结构的药品,也是目前在国际上获得广泛认可的中国原创药品.至今已被多个亚非国家指定为疟疾治疗一线用药,它在疟疾这一高传染性疾病治疗史上具有里程碑意义.其主要成分是青蒿素(是一种由青蒿中分离得到的具有新型化学结构的抗疟药),结构如图所示.有关该化合物的叙述正确的是( )| A、分子式为:C15H24O5 |
| B、该化合物在一定条件下不能与NaOH溶液反应 |
| C、该化合物中含有过氧键,一定条件下有氧化性 |
| D、青蒿素与维生素一样是水溶性的 |
下列实验操作错误的是( )
| A、进行分液操作时,分液漏斗中下层液体从下口放出 上层液体从上口倒出 |
| B、进行蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶支管口处 |
| C、进行分液操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
| D、进行蒸发操作时,不能使混合物中的水分完全蒸干 |
X、Y、Z三种元素的原子,其最外层电子排布为ns1,3s23p1和2s22p4,由这三种元素组成的化合物的化学式可能是( )
| A、X3YZ3 |
| B、X2YZ2 |
| C、XYZ2 |
| D、XYZ3 |
下列说法中正确的是( )
| A、共价化合物中一定只含有极性共价键 |
| B、只含有共价键的物质一定是共价化合物 |
| C、离子化合物中可能含有极性共价键或非极性共价键 |
| D、有较强共价键存在的物质熔沸点一定很高 |