题目内容
 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,
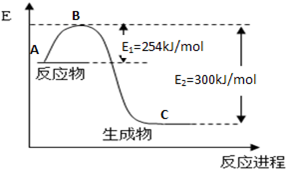
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,(1)如图是N2(g)和H2(g)反应生成1mol NH3(g)过程中能量变化示意图,请写出N2和H2反应的热化学方程式:
(2)若已知下列数据:
| 化学键 | H-H | N≡N |
| 键能/kJ?mol-1 | 435 | 943 |
(3)合成氨反应通常用铁触媒作催化剂.使用铁触媒后E1和E2的变化是:E1
(4)用NH3催化还原NOX还可以消除氮氧化物的污染.例如
4NH3(g)+3O2(g)=2N2(g)+6H2O(g);△H1=akJ/mol
N2(g)+O2(g)=2NO(g);△H2=bkJ/mol
若1mol NH3还原NO至N2,则该反应过程中的反应热△H3=
分析:(1)先求出此反应的焓变,根据热化学方程式的书写规则再写出热化学方程式;
(2)根据反应热等于反应物的总键能减去生成物的总键能计算;
(3)加入催化剂,反应物和生成物的活化能都降低;
(4)利用盖斯定律计算.
(2)根据反应热等于反应物的总键能减去生成物的总键能计算;
(3)加入催化剂,反应物和生成物的活化能都降低;
(4)利用盖斯定律计算.
解答:解:(1)反应物总能量大于生成物总能量,应为放热反应,生成1mol氨气放出46kJ热量,则反应的热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-92kJ/mol,
故答案为:N2(g)+3H2(g)?2NH3(g)△H=-92kJ/mol;
(2)反应热等于反应物的总键能减去生成物的总键能,设N-H的键能为x,
则943+3×435-6x=-92,x=390,故答案为:390;
(3)加入催化剂,反应物和生成物的活化能都降低,故答案为:减小;减小;
(4)已知①4NH3(g)+3O2(g)=2N2(g)+6H2O(g);△H1=akJ/mol
②N2(g)+O2(g)=2NO(g);△H2=bkJ/mol
利用盖斯定律将
可得NH3(g)+
NO(g)=
N2(g)+
H2O(g)△H3=
kJ/mol,
故答案为:
.
故答案为:N2(g)+3H2(g)?2NH3(g)△H=-92kJ/mol;
(2)反应热等于反应物的总键能减去生成物的总键能,设N-H的键能为x,
则943+3×435-6x=-92,x=390,故答案为:390;
(3)加入催化剂,反应物和生成物的活化能都降低,故答案为:减小;减小;
(4)已知①4NH3(g)+3O2(g)=2N2(g)+6H2O(g);△H1=akJ/mol
②N2(g)+O2(g)=2NO(g);△H2=bkJ/mol
利用盖斯定律将
| ①-3② |
| 4 |
| 3 |
| 2 |
| 5 |
| 4 |
| 3 |
| 2 |
| a-3b |
| 4 |
故答案为:
| a-3b |
| 4 |
点评:本题考查综合考查化学反应与能量变化知识,注意物质的总能量、键能与反应热的计算关系,把握盖斯定律的计算方法,题目难度中等.

练习册系列答案
 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案
相关题目
 氮是地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义.
氮是地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义.