题目内容
298K 100kPa时,NH3(g)+HCl(g)═NH4Cl(s)△H1=-176kJ?mol-1N2(g)+3H2(g)═2NH3(g)△H2=-92.2kJ?mol-1
H2(g)+Cl2(g)═2HCl(g)△H3=-184.6kJ?mol-1
298K时的N2(g)+4H2(g)+Cl2(g)═2NH4Cl(s)△H=______.
【答案】分析:由盖斯定律可知,一个反应一步完成和分步完成其反应热相同,则利用目标反应与已知反应的关系,将反应相加和或相减时,对应的反应热也应相加和或相减来计算.
解答:解:298K 100kPa时,NH3(g)+HCl(g)═NH4Cl(s)△H1=-176kJ?mol-1、、、、、、①,
N2(g)+3H2(g)═2NH3(g)△H2=-92.2kJ?mol-1、、、、、、②,
H2(g)+Cl2(g)═2HCl(g)△H3=-184.6kJ?mol-1、、、、、、③,
则由盖斯定律可知,
298K时的N2(g)+4H2(g)+Cl2(g)═2NH4Cl(s)可由②+③+①×2得到,
则△H=△H1×2+△H2+△H3=(-176kJ?mol-1)×2+(-92.2kJ?mol-1)+(-184.6kJ?mol-1)=-628.8kJ/mol,
故答案为:-628.8kJ/mol.
点评:本题考查学生利用盖斯定律来计算反应的反应热,明确已知反应和目标反应的关系是解答本题的关键,难度不大,注重了对高考热点的考查.
解答:解:298K 100kPa时,NH3(g)+HCl(g)═NH4Cl(s)△H1=-176kJ?mol-1、、、、、、①,
N2(g)+3H2(g)═2NH3(g)△H2=-92.2kJ?mol-1、、、、、、②,
H2(g)+Cl2(g)═2HCl(g)△H3=-184.6kJ?mol-1、、、、、、③,
则由盖斯定律可知,
298K时的N2(g)+4H2(g)+Cl2(g)═2NH4Cl(s)可由②+③+①×2得到,
则△H=△H1×2+△H2+△H3=(-176kJ?mol-1)×2+(-92.2kJ?mol-1)+(-184.6kJ?mol-1)=-628.8kJ/mol,
故答案为:-628.8kJ/mol.
点评:本题考查学生利用盖斯定律来计算反应的反应热,明确已知反应和目标反应的关系是解答本题的关键,难度不大,注重了对高考热点的考查.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
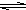 HS-+OH-
HS-+OH-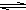 Al(OH)3+3H+有无色气体和白色絮状沉淀产生
Al(OH)3+3H+有无色气体和白色絮状沉淀产生