题目内容
5.现欲提取溴水中的溴单质,需进行以下操作:(1)可选用下列B物质为萃取剂.
A、酒精
B、苯(密度比水小)
C、KBr溶液
(2)萃取后静置一段时间,观察现象,上层为(填主要物质)溶有溴的苯,下层为水;
(3)分液时,应(填写液体如何分出)先让下层液体从下管口流出,再把上层液体从上口倒 出(直接转移到蒸馏烧瓶中);
(4)分液后,应进行(填操作方法)蒸馏即可得到溴单质.
分析 (1)根据萃取剂的选择必须符合下列条件:溶质在萃取剂中的溶解度比在原溶剂中要大;萃取剂与原溶剂不相溶;萃取剂与溶质不反应;
(2)溴在苯中溶解度远大于在水中的溶解度且苯的密度比水的小;
(3)分液时,避免上下层液体混合;
(4)溴单质和苯的沸点不同.
解答 解:(1)不能选用A,酒精与水互溶;不能选用C,溴水与KBr溶液互溶;可选用苯,故答案为:B;
(2)溴在苯中溶解度远大于在水中的溶解度且苯的密度比水的小,溶有溴的苯在上层,故答案为:溶有溴的苯;水;
(3)分液时,避免上下层液体混合,则应先从分液漏斗的下口放出下层液体,再从上口倒出上层液体,故答案为:先让下层液体从下管口流出,再把上层液体从上口倒出(直接转移到蒸馏烧瓶中);
(4)溴单质和苯的沸点不同,对溴的苯溶液进行蒸馏,溴极易挥发,可用蒸馏分离,故答案为:蒸馏.
点评 本题考查分液与萃取,为高频考点,涉及实验基本操作和混合物分离提纯方法,注重实验技能的考查,注意实验操作的评价性分析,题目难度不大.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
15.已知镁粉与冷水几乎不反应,与热水反应缓慢.市场上购买的“即热饭盒”底部有两层,一层装水,另一层是镁粉与铁粉的混合物,当水与金属粉末接触时会发生反应Mg+2H2O═Mg(OH)2+H2↑.则下列说法不正确的是( )
| A. | “即热饭盒”的工作原理是将化学能转化为热能 | |
| B. | 上述反应中,反应物的总焓大于生成物的总焓 | |
| C. | 铁粉的作用是催化剂 | |
| D. | 上述反应的反应热Q为正值 |
13.下列化工生产过程中,需用到电解食盐水产物的是 ( )
| A. | 工业生产纯碱 | B. | 金属铝的冶炼 | C. | 海水中提取溴 | D. | 工业生产玻璃 |
20.如表为元素周期表的一部分,请参考元素①-⑦在表中的位置,用元素符号或化学用语回答下列问题:
(1)①和②形式的最简有机化合物分子的结构式为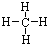
(2)下列事实能证明②的非金属性比⑥强的是CD
A:Na2CO3+SiO2$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑;
B:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑
C:Na2SiO3+CO2+2H2O═H2SiO3↓+Na2CO3;
D:CH4比SiH4稳定
(3)写出①、③、④三种元素组成化合物的电子式
(4)③、④、⑤的形式的简单离子半径依次减小(填“增大”、“减小”或“不变”)
(5)①、②、⑦三种元素按原子个数之比为11:5:1组成的有机化合物中含有两个-CH3的同分异构体有4种.
| 族 | LA | 0 | ||||||
| 周期 | ||||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ||||

(2)下列事实能证明②的非金属性比⑥强的是CD
A:Na2CO3+SiO2$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑;
B:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑
C:Na2SiO3+CO2+2H2O═H2SiO3↓+Na2CO3;
D:CH4比SiH4稳定
(3)写出①、③、④三种元素组成化合物的电子式

(4)③、④、⑤的形式的简单离子半径依次减小(填“增大”、“减小”或“不变”)
(5)①、②、⑦三种元素按原子个数之比为11:5:1组成的有机化合物中含有两个-CH3的同分异构体有4种.
10.下列物质中不能用来区分乙酸、乙醇、苯、四氯化碳的是( )
| A. | 溴水 | B. | 酸性髙锰酸钾溶液 | ||
| C. | 碳酸钠溶液 | D. | 紫色石蕊溶液 |
17.下列有关物质变化的说法不正确的是( )
| A. | 煤的液化和气化都是化学变化 | |
| B. | 硝化反应和酯化反应都属于取代反应 | |
| C. | 石油的分馏和裂化都是化学反应 | |
| D. | 乙烯与溴和水的反应都属于加成反应 |
14.反应2SO2+O2?2SO3(g)经一段时间后,SO3的浓度增加了0.2mol/L,在这段时间内用O2表示的反应速率为0.01mol•L-1•s-1,则这段时间为( )
| A. | 0.1s | B. | 2.5s | C. | 5s | D. | 10s |
9.某盐是一种重要的化工原料,在印染、制革、木材和农业等领域有重要用途,其溶液可能含有NH4+、Al3+、SO42-、Fe2+、Cl-等若干种离子,某同学设计并完成了如下实验:
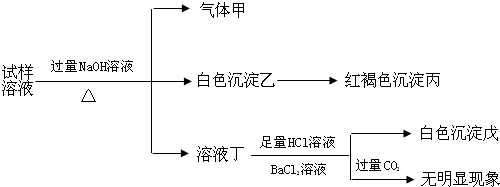
根据以上的实验操作与现象,该同学得出的结论不正确的是( )

根据以上的实验操作与现象,该同学得出的结论不正确的是( )
| A. | 试样中肯定有NH4+、SO42-和Fe2+ | |
| B. | 试样中一定没有Al3+ | |
| C. | 若气体甲在标准状况下体积为0.448L,沉淀丙和沉淀戊分别为1.07g和4.66g,则可判断溶液中还有Cl- | |
| D. | 该盐工业上可以用作净水剂 |
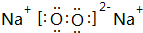 ,其中含有的化学键为离子键和共价键;
,其中含有的化学键为离子键和共价键;