题目内容
6.NA为阿伏加德罗常数,下列物质所含分子数最多的是( )| A. | 标准状况下2.24LO2 | B. | 含NA个氢原子的H2 | ||
| C. | 44gCO2 | D. | 含3.01×1023个分子的CH4 |
分析 根据n=$\frac{V}{{V}_{m}}$计算氧气物质的量,根据n=$\frac{m}{M}$计算二氧化碳物质的量,根据n=$\frac{N}{{N}_{A}}$计算氢气、甲烷物质的量,根据N=nNA可知,物质的量越大含有分子数目越多.
解答 解:A.标准状况下2.24LO2的物质的量为$\frac{2.24L}{22.4L/mol}$=0.1mol;
B.NA个氢原子的物质的量为1mol,则H2的物质的量为0.5mol;
C.44gCO2的物质的量为$\frac{44g}{44g/mol}$=1mol;
D.3.01×1023个CH4分子的物质的量为$\frac{3.01×1{0}^{23}}{6.02×1{0}^{23}mo{l}^{-1}}$=0.5mol,
故44gCO2含有分子数目最多,
故选:C.
点评 本题考查物质的量有关计算,比较基础,注意对基础知识的理解掌握与灵活应用.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
16.有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的:
为了鉴别上述化合物,分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,仅有B为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸酸化的硝酸钡溶液,只有A中放出无色气体,只有D中产生白色沉淀;
⑤将B、C两溶液混合,未见沉淀或气体生成.根据上述实验填空:
(1)写出B、D的化学式:BKCl,DCuSO4.
(2)C可用作净水剂,用离子方程式表示其净水原理Al3++3H2O?Al(OH)3(胶体)+3H+.
(3)将含0.01mol A的溶液与含0.02mol E的溶液反应后,向溶液中滴加0.1mol•L-1稀盐酸.下列图象能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是C

(4)在m mL b mol•L-1 C溶液中,加入等体积a mol•L-1 的E溶液.当a≤3b时,生成沉淀的物质的量是$\frac{ma}{3}$×10-3 mol;当3b<a<4b件时,生成沉淀的物质的量是(4mb-ma)×10-3mol.
| 阳离子 | K+ Na+ Cu2+ Al3+ |
| 阴离子 | SO42- HCO3-OH- Cl- |
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,仅有B为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸酸化的硝酸钡溶液,只有A中放出无色气体,只有D中产生白色沉淀;
⑤将B、C两溶液混合,未见沉淀或气体生成.根据上述实验填空:
(1)写出B、D的化学式:BKCl,DCuSO4.
(2)C可用作净水剂,用离子方程式表示其净水原理Al3++3H2O?Al(OH)3(胶体)+3H+.
(3)将含0.01mol A的溶液与含0.02mol E的溶液反应后,向溶液中滴加0.1mol•L-1稀盐酸.下列图象能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是C

(4)在m mL b mol•L-1 C溶液中,加入等体积a mol•L-1 的E溶液.当a≤3b时,生成沉淀的物质的量是$\frac{ma}{3}$×10-3 mol;当3b<a<4b件时,生成沉淀的物质的量是(4mb-ma)×10-3mol.
14.25℃时,下列说法正确的是( )
| A. | pH=2的醋酸溶液与pH=12的氢氧化钠溶液等体积混合,混合后溶液pH=7 | |
| B. | 将0.1mol•L-1氢氧化钠溶液与pH=1稀硫酸等体积混合,混合后的溶液pH<7 | |
| C. | 硫酸铵溶液中:c(SO42-)>c(NH4+)>c(H+)>c(OH-) | |
| D. | pH相同的醋酸钠溶液、碳酸氢钠溶液、碳酸钠溶液,其物质的量浓度: c(CH3COONa)>c(NaHCO3)>c(Na2CO3) |
11.X、Y、Z、M、N是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如表:
(1)M在元素周期表中的位置为第三周期ⅥA族. X的最高价氧化物的电子式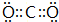 .
.
(2)标准状况下,将4.48L X的最高价氧化物通入1L 0.3mol•L-1 Z的最高价氧化物对应水化物的溶液中发生反应的离子方程式为3OH-+2CO2=HCO3-+CO32-+H2O.
(3)Y的氢化物Y2H4是火箭的常见燃料,已知16.0g该液态燃料在氧气中完全燃烧生成氮气和液态水时,放出312kJ热量.写出该反应的热化学方程式:N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-624 kJ•mol-1.
(4)元素N与人体分泌物中的盐酸以及空气反应可生成超氧酸(HO2):N+HCl+O2═NCl+HO2,HO2不仅是一种弱酸而且也是一种自由基,具有极高的活性.下列有关该反应的说法错误的是C.
A.氧化剂是O2
B.HO2在碱中不能稳定存在
C.氧化产物是HO2
D.1mol N参加反应就有1mol电子发生转移
(5)Y、Z两元素形成的化合物H可用于汽车的安全气囊,取6.5g H充分撞击分解后得到两种单质,其中一种气体单质的体积在标准状况下为3.36L,则H的化学式为NaN3,该物质的晶体类型为离子晶体.
| 元素 | 相关信息 |
| X | X元素可形成自然界中硬度最大的物质 |
| Y | 其单质为双原子分子,其最简单氢化物的水溶液能使酚酞变红 |
| Z | Z是短周期内最容易失去电子的元素 |
| M | M的一种同位素的质量数为34,中子数为18 |
| N | N是具有紫红色光泽的金属,有很好的延展性、导热性和导电性 |
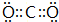 .
.(2)标准状况下,将4.48L X的最高价氧化物通入1L 0.3mol•L-1 Z的最高价氧化物对应水化物的溶液中发生反应的离子方程式为3OH-+2CO2=HCO3-+CO32-+H2O.
(3)Y的氢化物Y2H4是火箭的常见燃料,已知16.0g该液态燃料在氧气中完全燃烧生成氮气和液态水时,放出312kJ热量.写出该反应的热化学方程式:N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-624 kJ•mol-1.
(4)元素N与人体分泌物中的盐酸以及空气反应可生成超氧酸(HO2):N+HCl+O2═NCl+HO2,HO2不仅是一种弱酸而且也是一种自由基,具有极高的活性.下列有关该反应的说法错误的是C.
A.氧化剂是O2
B.HO2在碱中不能稳定存在
C.氧化产物是HO2
D.1mol N参加反应就有1mol电子发生转移
(5)Y、Z两元素形成的化合物H可用于汽车的安全气囊,取6.5g H充分撞击分解后得到两种单质,其中一种气体单质的体积在标准状况下为3.36L,则H的化学式为NaN3,该物质的晶体类型为离子晶体.
16.已知常温下几种酸的电离常数如表所示:
(1)写出铬酸的第二步电离的K2表达式:$\frac{[Cr{{O}_{4}}^{-}]•[{H}^{+}]}{[HCr{{O}_{4}}^{-}]}$.
(2)常温下,KCN的水解常数Kh为2.0×10-5.
(3)常温下,浓度相同的K2S、K2SO3、K2CrO4三种水溶液中,水电离程度最大的是K2S.
(4)常温下,0.1mol•L-1氢硫酸溶液中离子浓度大小排序为H+>HS->S2+>OH-,.
(5)H2SO3第二步电离常数小于第一步电离常数,其主要原因是H2SO3第一步电离产生的氢离子会抑制第二步电离.
(6)已知常温下,Ksp(Ag2CrO4)=1.12×10-12,Ksp(BaCrO4)=1.17×10-10.在浓度都为0.001mol•L-1的含Ag+、Ba2+的溶液中,缓慢滴加稀K2CrO4溶液,先产生的沉淀的化学式是BaCrO4.
| 酸的化学式 电离常数K | 氢硫酸 H2S | 亚硫酸 H2SO3 | 铬酸 H2CrO4 | 氰酸 HCN |
| K1 | 9.1×10-8 | 1.5×10-2 | 1.8×10-1 | 5.0×10-10 |
| K2 | 1.1×10-12 | 1.0×10-7 | 3.2×10-7 |
(2)常温下,KCN的水解常数Kh为2.0×10-5.
(3)常温下,浓度相同的K2S、K2SO3、K2CrO4三种水溶液中,水电离程度最大的是K2S.
(4)常温下,0.1mol•L-1氢硫酸溶液中离子浓度大小排序为H+>HS->S2+>OH-,.
(5)H2SO3第二步电离常数小于第一步电离常数,其主要原因是H2SO3第一步电离产生的氢离子会抑制第二步电离.
(6)已知常温下,Ksp(Ag2CrO4)=1.12×10-12,Ksp(BaCrO4)=1.17×10-10.在浓度都为0.001mol•L-1的含Ag+、Ba2+的溶液中,缓慢滴加稀K2CrO4溶液,先产生的沉淀的化学式是BaCrO4.
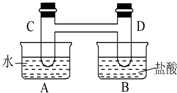 如图所示,在容器A中装有20℃的水50mL,容器B中装有1 mol/L的盐酸50mL,试管C、D相连通,且其中装有红棕色NO2和无色N2O4的混合气体,并处于下列平衡:
如图所示,在容器A中装有20℃的水50mL,容器B中装有1 mol/L的盐酸50mL,试管C、D相连通,且其中装有红棕色NO2和无色N2O4的混合气体,并处于下列平衡: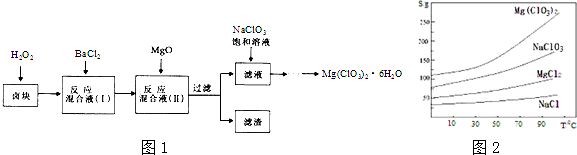
 已知常温下甲醛是一种无色、有刺激性气味的气体,易溶于水,是世界卫生组织(WHO)确认的致癌物和致畸物质之一.我国规定:居室中甲醛含量不得超过0.08mg/m3.可利用酸性高锰酸钾溶液测定甲醛含量.
已知常温下甲醛是一种无色、有刺激性气味的气体,易溶于水,是世界卫生组织(WHO)确认的致癌物和致畸物质之一.我国规定:居室中甲醛含量不得超过0.08mg/m3.可利用酸性高锰酸钾溶液测定甲醛含量. .
.