题目内容
25℃时,水的电离达到电离平衡:H20?H++OH-△H>0,下列操作会抑制H20的电离,且pH>7的是( )
| A、向水中加少量Na2C03 |
| B、向水中加少量NaOH |
| C、向水中加少量FeCl3 |
| D、将水加热到90℃ |
考点:水的电离
专题:电离平衡与溶液的pH专题
分析:欲使水的电离平衡向逆方向移动,并使c(H+)减小,pH增大,可加入碱,抑制水的电离,溶液PH增大,以此解答该题.
解答:
解:A.碳酸钠水解能促进水电离,溶液中c(H+)减小,pH增大,故A错误;
B.加入氢氧化钠抑制水电离,c(H+)减小,pH增大,故B正确;
C.向水中加少量FeCl3水解促进水电离,溶液呈酸性,pH减小,故C错误;
D.水的电离是吸热过程,加热促进电离,c(H+)增大,PH减小,故D错误;
故选B.
B.加入氢氧化钠抑制水电离,c(H+)减小,pH增大,故B正确;
C.向水中加少量FeCl3水解促进水电离,溶液呈酸性,pH减小,故C错误;
D.水的电离是吸热过程,加热促进电离,c(H+)增大,PH减小,故D错误;
故选B.
点评:本题考查弱电解质的电离,题目难度不大,注意影响弱电解质电离的因素,从平衡移动的角度分析.

练习册系列答案
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案
相关题目
下列叙述中,正确的是( )
| A、漂白粉、纯碱、淀粉、氢氧化铁胶体分别属于混合物、盐、有机物、纯净物 |
| B、离子键属于静电作用,离子化合物属于电解质 |
| C、碳单质仅2种同素异形体 |
| D、单斜硫和斜方硫是硫的两种同位素 |
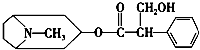 中国科学家从中药材中提取的金丝桃素对人工感染的H5N1亚型禽流感家禽活体具有良好的治愈率,从而在防治禽流感药物研究方面取得重大突破.已知金丝桃素的结构简式如图所示,下列有关说法正确的是( )
中国科学家从中药材中提取的金丝桃素对人工感染的H5N1亚型禽流感家禽活体具有良好的治愈率,从而在防治禽流感药物研究方面取得重大突破.已知金丝桃素的结构简式如图所示,下列有关说法正确的是( )| A、金丝桃素的分子式为C17H22O3N |
| B、金丝桃素能在NaOH溶液中加热反应得到两种芳香族化合物 |
| C、在加热条件下金丝桃素能与浓硫酸和浓硝酸的混合液发生取代反应 |
| D、1mol金丝桃素最多能与4mol H2发生加成反应 |
某氯原子的质量为a g,12C原子的质量为b g,用NA表示阿伏加德罗常数的值,下列说法中不正确的是( )
| A、该氯原子的摩尔质量为12a/b |
| B、x g该氯原子的物质的量一定是x/(a×NA)mol |
| C、1mol该氯原子的质量是aNAg |
| D、y g该氯原子所含的原子数为y/a个 |
下列溶液中能大量共存的离子组是( )
| A、加入铝粉能放出氢气的溶液中:K+、Ba2+、Cl-、Br- | ||
B、某无色透明溶液中 Cu2+、Na+、Cl-、HCO
| ||
| C、含有大量Fe3+的溶液:SCN-、I-、K+、Br- | ||
| D、在pH=1的溶液中:ClO-、NH4+、K+、Cl- |
反应2SO2+O2
2SO3是工业上制造硫酸的重要反应.下列关于该反应的说法正确的是( )
| 一定条件 |
| A、降低体系温度能加快反应速率 |
| B、增加SO3的浓度不能加快反应速率 |
| C、加入新型高效催化剂,可以使SO2转化率达到100% |
| D、一定条件下达到该反应进行的限度即指SO2转化为SO3的速率与SO3转化为SO2的速率相等 |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、7.8g苯中含有0.3NA个碳碳双键,0.3NA个碳碳单键 |
| B、2L 0.1 mol/L的醋酸钠溶液中,醋酸根离子数为0.2NA |
| C、5.6g铁与足量的稀硝酸反应,失去电子数为0.2NA |
| D、SiO2晶体中,有NA个Si就有4NA个Si-O键 |