题目内容
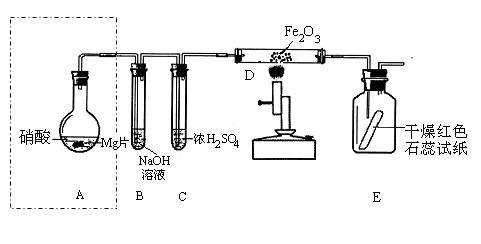
下列实验现象或结果一定不可能出现的是
[ ]
A.向NaI溶液中滴加几滴AgNO3溶液,产生黄色沉淀,再加入稀硝酸,沉淀不溶解,但溶液由无色变为黄色
B.向浓HNO3中滴加紫色石蕊试液,加热最终变为无色溶液
C.向稀盐酸中滴加NaAlO2溶液,无沉淀产生
D.讨量的Fe在氯气中燃烧,最终产物是FeCl2
B.向浓HNO3中滴加紫色石蕊试液,加热最终变为无色溶液
C.向稀盐酸中滴加NaAlO2溶液,无沉淀产生
D.讨量的Fe在氯气中燃烧,最终产物是FeCl2
D

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

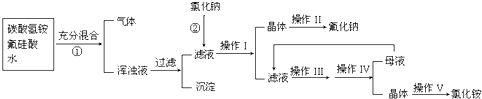
 (4)目前工业上正积极探索用浓HNO3作氧化剂,用Cu与浓H2SO4、浓HNO3反应,采取间歇加热、逐渐加入浓HNO3的方法来制备CuSO4•5H2O的新工艺。模拟制备装置如下图所示。
(4)目前工业上正积极探索用浓HNO3作氧化剂,用Cu与浓H2SO4、浓HNO3反应,采取间歇加热、逐渐加入浓HNO3的方法来制备CuSO4•5H2O的新工艺。模拟制备装置如下图所示。