题目内容
充分煅烧黄铁矿W g,反应完全后冷却至室温,称得固体物质的质量是m g,生成SO2为V L,则黄铁矿中FeS2的含量是(假设矿石中的杂质受热不分解,也不会与SO2反应)( )A.![]() ×100% B.
×100% B.![]() ×100%
×100%
C.![]() ×100% D.
×100% D.![]() ×100%
×100%
解析:本题可用两种方法求解。
解法一:此题可根据化学方程式进行计算,因得到的SO2为室温下体积,故应用固体质量之差进行计算。
设黄铁矿中FeS2的质量分数是x。
4FeS2+11O2![]() 2Fe2O3+8SO2? Δm
2Fe2O3+8SO2? Δm
480 320 160
? Wg×x (W-m)g
![]()
解得x=![]() ×100%,故选D。
×100%,故选D。
解法二:本题可不通过计算,直接判断。因为室温下得SO2的体积为V L,故不能根据标准状况下用V值进行有关计算,而4个选项中不涉及V值的只有D。

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
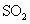 P(g),假设杂质在煅烧过程中不参加反应,黄铁矿的质量分数可表示为
P(g),假设杂质在煅烧过程中不参加反应,黄铁矿的质量分数可表示为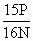 ×100%
×100%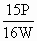 ×100%
×100%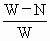 ×100%
×100%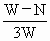 ×100%
×100%