题目内容
选做[物质结构与性质](10分)
已知X、Y、Z、Q、E五种元素的原子序数依次增大,其中X原子核外电子有6种不同的运动状态,s能级电子数是P能级电子数的两倍;Z原子L层上有2对成对电子;Q是第三周期中电负性最大的元素;E+的M层3d轨道电子全充满。请回答下列问题:
(1)X、Y、Z第一电离能由小到大的顺序为______ <______<______ (填元素符号)。
<______<______ (填元素符号)。
(2)E元素基态原子的电子排布式为________________________________。
(3)XZ2的分子中含有 个π键。
(4)Z氢化物的沸点比Q氢化物的沸点高,理由是____________ 。
(5)将YH3通入灼热EZ中发现黑色固体变红色,生成物对大气不造成污染。请写出有关化学方程式 。
(1)C<O<N (2) ls22s22p63s23p63d104s1 (3) 2
(4)H2O分子间能形成氢键,HCl分子间不能形成氢键
(5)3CuO+2NH3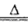 3Cu+3H2O+N2(要加热条件)
3Cu+3H2O+N2(要加热条件)
【解析】
试题分析:X原子核外电子有6种不同的运动状态,即X原子有6个电子,所以X是C元素;Z原子L层上有2对成对电子,则L层电子数是6个,所以Z是O元素,则Y是N元素;Q是第三周期中电负性最大的元素,第三周期电负性最大的元素是Cl,则Q是Cl元素;E+的M层3d轨道电子全充满,则E元素原子的最外层是4s1,则E是Cu元素。
(1)同周期元素的第一电离能随核电荷数的增加而增大,但N元素原子的2p轨道是3个电子,为半充满的稳定状态,则N>O,所以X、Y、Z第一电离能由小到大的顺序为C<O<N;
(2)Cu元素核外有29个电子,根据电子的排布规律,Cu基态原子的电子排布式为ls22s22p63s23p63d104s1;
(3)CO2分子中,C与O原子之间形成C=O双键,所以共有2个π键;
(4)O氢化物的沸点比Cl氢化物的沸点高,是因为水分子间存在氢键,使沸点升高;
(5)将NH3通入灼热CuO中发现黑色固体变红色,生成物对大气不造成污染,则红色固体为Cu,其余产物为氮气和水,所以反应的化学方程式为3CuO+2NH3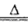 3Cu+3H2O+N2。
3Cu+3H2O+N2。
考点:考查元素的推断,物质结构与性质的应用

 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案 2H2O+O2↑ D.CaCO3
2H2O+O2↑ D.CaCO3 CaO+CO2↑
CaO+CO2↑ 。
。