题目内容
酸、碱、盐都是电解质,在水中都能电离出离子。根据下列化合物:(1)NaOH(2)CH3COOH(3)NH4Cl(4)NH3·H2O(5)CH3COONa请回答下列问题: (1)上述几种电解质中属于弱电解质的是 ,溶液呈酸性的有 (填序号) (2)常温下0.01mol/L NaOH溶液的PH= ;PH=11的CH3COONa溶液中由水电离产生的c(OH-) = (3)用离子方程式表示NH4Cl溶液呈酸性的原因 ,其溶液中离子浓度按由大到小的顺序为 (4)将等PH等体积的NaOH和NH3·H2O分别稀释m倍和n倍,稀释后两溶液的PH仍相等,则m n (填“大于、等于、小于”) (5)常温下,向100 mL 0.01 mol·L-1HA溶液中逐滴加入0.02 mol·L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题: 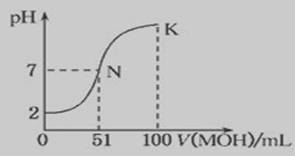
①由图中信息可知HA为________酸(填“强”或“弱”),理由是____________ 。
② K点对应的溶液中,c(M+)+c(MOH)________2c(A-)(填“>”、“<”或“=”)。
(1)(2)(4) 、(2)(3)
(2) 12 、 10-3 mol/L
(3)NH4+ + H2O ![]() NH3·H2O + H+、c(Cl-)>c(NH4+)>c(H+)>c(OH-)
NH3·H2O + H+、c(Cl-)>c(NH4+)>c(H+)>c(OH-)
(4) 小于
(5)① 强 、 0.01 mol/LHA的PH =2 ② =

 酸、碱、盐都是电解质,在水中都能电离出离子.根据下列化合物:
酸、碱、盐都是电解质,在水中都能电离出离子.根据下列化合物: