��Ŀ����
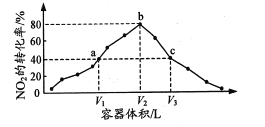
����Ŀ���¶�ΪT�棬��������ȵĺ����ܱ������зֱ������������̿��1mol NO2��������Ӧ��2C(s)+2NO2(g)N2(g)+2CO2(g)��Ӧ��ͬʱ�䣬��ø�������NO2��ת��������������Ĺ�ϵ��ͼ��ʾ������˵����ȷ����
A.T��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��Ϊ![]()
B.ͼ��c����ʾ�����£�v(��)��v(��)
C.��a��ƽ����ϵ�г���һ������NO2���ﵽƽ��ʱ��NO2��ת���ʱ�ԭƽ���
D.�����ڵ�ѹǿ��Pa:Pb��6:7
���𰸡�BD
��������
�ɷ�Ӧ![]() ��֪�������Խ��ѹǿԽС����Ӧ���������ƶ���NO2��ת������ߣ���ͼ���֪����ͬʱ�䣬a��bΪ�Ѵﵽƽ��㣬c��δ�ﵽƽ�⣬���û�ѧƽ�ⳣ���͵�Чƽ����з�����
��֪�������Խ��ѹǿԽС����Ӧ���������ƶ���NO2��ת������ߣ���ͼ���֪����ͬʱ�䣬a��bΪ�Ѵﵽƽ��㣬c��δ�ﵽƽ�⣬���û�ѧƽ�ⳣ���͵�Чƽ����з�����
A. a��ʱ��Ӧ�ﵽƽ�⣬NO2ת����Ϊ40%����
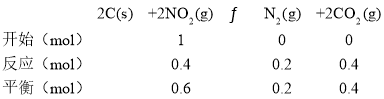
T��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��Ϊ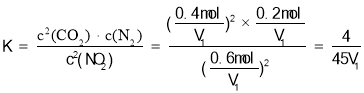 ����A����
����A����
B. ͼ��c�㻹δ�ﵽƽ�⣬��Ӧ����������У�v(��)��v(��)����B��ȷ��
C. ��a��ƽ����ϵ�г���һ������NO2����Ч�ڼ�ѹ��ƽ�����ƣ�ת���ʽ��ͣ�C����
D.��A��֪a��ʱ�������������ʵ���Ϊ1.2mol��b��ʱ��Ӧ����ʽΪ
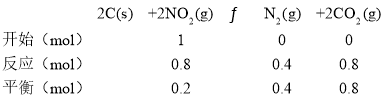
��b���������������ʵ���Ϊ1.4mol������V1��V2����Pa:Pb��6:7����D��ȷ��
�ʴ�ѡ��BD��

 ��ʦ����ɳ���ʱͬ��ѧ����ϵ�д�
��ʦ����ɳ���ʱͬ��ѧ����ϵ�д�����Ŀ������β����ȼúβ���������������Ҫԭ��֮һ��
(1)��ҵ�����ü������ԭNO���ɼ��ٵ���������ŷš�
��֪��CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ��H=-574kJ��mol1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ��H =-1160kJ��mol1
����ֱ�ӽ�NO2��ԭΪN2���Ȼ�ѧ����ʽΪ____________________________��
(2)��������β����Ⱦ��ԭ��Ϊ2NO(g)+2CO(g)![]() N2(g)+2CO2(g) ��H ��0������º����ܱ������г���NO��CO���ô�������õ��������±���ʾ��
N2(g)+2CO2(g) ��H ��0������º����ܱ������г���NO��CO���ô�������õ��������±���ʾ��
ʱ��/s | 0 | 1 | 2 | 3 | 4 |
c(NO)/��10-3mol��L1 | 9.00 | 4.00 | 2.00 | 1.00 | 1.00 |
c(CO)/��10-3mol��L1 | 9.00 | 4.00 | 2.00 | 1.00 | 1.00 |
��Ϊ�����β��������Ч�����ɲ�ȡ�Ĵ�ʩ��____________��д�����ּ��ɣ���
�ڴ������´ﵽƽ��ʱ������÷�Ӧ��ƽ�ⳣ��K=____________________��
(3)��ҵ��������������Һ��ͬʱ����SO2�͵�������������(NOx)���ɵõ�Na2SO3��NaHSO3��NaNO2��NaNO3����Һ������֪�������£�HNO2�ĵ��볣��ΪKa=7��10-4��H2SO3�ĵ��볣��ΪKa1=1.2��10-2��Ka2=5.8��10-8����
�ٳ����£���ͬŨ�ȵ�Na2SO3��NaNO2��Һ��pH�ϴ����________��Һ��
�ڳ����£�NaHSO3��_________�ԣ���ᡱ������С������жϵ�������________________________________________________��ͨ������˵������
(4)����(Ce)������+3��+4���ּ�̬��NO���Ա���Ce4+����Һ���գ�����NO2-��NO3-���������ʵ���֮��Ϊ1��1)���ɲ��õ�ⷨ����������Һ�е�NO2-ת��Ϊ�����ʣ�ͬʱ����Ce4+����ԭ����ͼ��ʾ��

��Ce4+�ӵ��۵�__________(����ĸ����)��������
��д�������ĵ缫��Ӧʽ______________________��
����Ŀ����������һ����;�ܹ�Ļ�����Ʒ�����Ժ�Σ����С���ǰ�ȫ�Ժܸߵ��л��ܼ�����������Ȼ���ϳ���֬����֬�����л������������ȶ��к�ǿ���ܽ�������������Ϊ���Ӽ���ϴ���Ͷ����л��ϳɲ��ϡ���ͨ�����·�Ӧԭ����ȡ�����ѣ�
2CH3CH2CH2CH2OH![]() CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
��֪������ʵIJ�����Ϣ���£�
�е�(��) | �ܶ�(g/cm3) | �ܽ��(g) | ��Է������� | |
������ | 117.7 | 0.81 | 7.9 | 74 |
������ | 142 | 0.77 | ������ˮ | 130 |
ij���⻯ѧѧϰС���������������������ʵ�鲽��ϳ������ѣ�
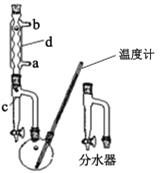
����100 mL������ƿ�м���30.0 mL��������5.0 mLŨ����ͼ�����ʯ�����ҡ�ȡ��ڷ�ˮ���м���3.0 mL����ʳ��ˮ����ͼ����װ��������ͨ����ˮ��
�ڷ�Ӧ���ڵ������ϼ��ȣ�ʹƿ��Һ���У�������ӦԼ1Сʱ������Һ������ˮ��ʱ����ˮ���ų�һ����ˮ����ˮ�㲻�ٱ仯��ƿ�з�Ӧ�¶ȴ�150 �棬��Ӧ��������ɣ�ֹͣ���ȣ�
��������ӦҺ��ȴ���·�ˮ�����������ij�����װ����ͼ�����ټӼ�����ʯ�������ռ���֣�
�ܾ��ƣ������Һ����ʢ��10 mLˮ�ķ�Һ©���У������ҡ��������ȥˮҺ���л���������5 mLˮ��3 mL 5% NaOH��Һ��3 mLˮ��3 mL�����Ȼ�����Һϴ�ӣ���ȥˮ�㣬���������ྻ�����С��ƿ�У�Ȼ�����0.2��0.4 9��ˮ�Ȼ��ƣ��ٽ�Һ��ת��װ�ñ��н��������ռ������9.0 mL��
��.  ��.
��. ![]() ��.
��.
��������ϲ����ش��������⣺
(1)�Ʊ������ѵķ�Ӧ������___������d��������____��
(2)�ڲ�����������Լ���˳����____�����װ���ң�װ�ü��ŵ��� ___��
(3)�ڲ�����в��õ������ȶ������þƾ���ֱ�Ӽ��ȵ�ԭ�������____��
(4)�ڲ�������ռ�������˵��¶ȷ�ΧΪ____(����ȷ�𰸱��)��
A.115�桫ll9�� B.140�桫144�� C. 148�桫152��
(5)�ھ����У��л�����____��(����������������)��������ˮ�Ȼ��Ƶ�������____��
(6)��С��ʵ������������ѵIJ���ԼΪ ___%(����������һλС��)��