题目内容
|
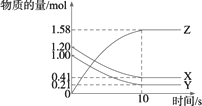
一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列描述正确的是
| |
A. |
反应开始到10 s,用Z表示的平均反应速率为0.158 mol·(L·s)-1 |
B. |
反应开始到10 s,X的物质的量浓度减少了0.79 mol·L-1 |
C. |
反应开始到10 s时,Y的转化率为79.0% |
D. |
反应的化学方程式为:X(g)+Y(g) |
答案:C
解析:
解析:
|
根据题图所示,X、Y的物质的量随时间逐渐减少,Z的物质的量逐渐增多,在10 s时达到平衡,由此可见X、Y为反应物,Z为生成物.在0-10 s内,Z增加了1.58 mol,X减少了(1.20-0.41)=0.79 mol,Y减少了(1.00-0.21)=0.79 mol,根据化学反应方程式的计量数之比等于其物质的量浓度的变化之比得X+Y |

练习册系列答案
 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目


 Z(g)
Z(g)

 Z(g)
Z(g)