题目内容
11.常温下,下列溶液的离子浓度关系式正确的是( )| A. | pH=4的氯化铵溶液中:c(H+)=c(NH3•H2O )=1×10-4mol•L-1 | |
| B. | pH相同的①NaOH、②NaClO两种溶液中水的电离程度:①<② | |
| C. | pH=2的HF溶液与pH=12的NaOH溶液以体积比1:1混合:c(Na+)=c(F-)>c(H+)=c(OH-) | |
| D. | pH=a的HCl溶液,稀释10倍后,其pH=b,则a=b-1 |
分析 A.NH4+水解生成NH3•H2O,且水解程度不大,水解显酸性;
B.NaOH抑制水的电离,而NaClO促进水的电离;
C.等体积混合后,溶液的溶质为NaF、HF,溶液显酸性;
D.HCl为强酸,稀释10倍后,pH增大1个单位.
解答 解:A.NH4+水解生成NH3•H2O,且水解程度不大,水解显酸性,则c(H+)=1×10-4mol•L-1>c(NH3•H2O ),故A错误;
B.NaOH抑制水的电离,而NaClO促进水的电离,则两种溶液中水的电离程度:①<②,故B正确;
C.等体积混合后,溶液的溶质为NaF、HF,溶液显酸性,则离子浓度为c(F-)>c(Na+)>c(H+)>c(OH-),故C错误;
D.HCl为强酸,稀释10倍后,pH增大,则pH=a的HCl溶液,稀释10倍后,其pH=b,可知a=b-1,故D正确;
故选BD.
点评 本题考查离子浓度的比较及盐类水解,为高频考点,把握电离与水解、酸碱混合后离子浓度关系为解答的关键,侧重分析与应用能力的考查,注意选项C为解答的易错点,题目难度不大.

练习册系列答案
相关题目
12.设NA为阿伏加德罗常数的值,下列说法不正确的是( )
| A. | 9.2g NO2和N2O4的混合物中含氮原子数目为0.2NA | |
| B. | 常温常压下,35.5g Cl2与足量的NaOH溶液完全反应,转移的电子数为NA | |
| C. | 标准状况下,2.24L NH3与1.6g CH4分子中所含电子数目均为NA | |
| D. | 已知反应N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ•mol-1,当生成NA个NH3分子时,反应放出的热量小于46.2kJ |
19.基于以下实验现象,下列实验操作和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 测定常温时的饱和HCOONa溶液、CH3COONa溶液的pH | HCOONa的pH<CH3COONa的pH | 弱酸的酸性:HCOOH>CH3COOH |
| B | 向5ml 2mol•L-1NaOH溶液中加入1ml 1mol•L-1CuSO4溶液,振荡后加入0.5ml有机物X,加热 | 未出现砖红色沉淀 | 说明X中不含有醛基 |
| C | KBrO3溶液中加入少量苯,然后通入少量Cl2 | 有机相呈橙红色 | 氧化性:Cl2>Br2 |
| D | NaAlO2溶液与NaHCO3溶液混合 | 有白色絮状沉淀生成 | 二者水解相互促进生成氧化铝沉淀 |
| A. | A | B. | B | C. | C | D. | D |
16.某有机物的结构简式如图.下列关于该物质的说法中正确的是( )
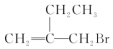
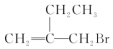
| A. | 该物质可以发生水解反应 | |
| B. | 该物质能和AgNO3溶液反应产生AgBr沉淀 | |
| C. | 该物质可以发生消去反应 | |
| D. | 该物质不能使溴的四氯化碳溶液褪色 |
3.R、X、Y、Z、W是短周期主族元素,它们在元素周期表中的相对位置如表所示.R最高价氧化物对应水化物与其简单气态氢化物反应可以形成离子化合物.下列推断正确的是( )
| R | X | Y |
| Z | W |
| A. | 最简单气态氢化物的热稳定性由强到弱的排序:Z、R、X、Y | |
| B. | R、X、Y、Z、W各元素最高价和最低价的绝对值之和均为8 | |
| C. | 最高价氧化物的水化物酸性由弱到强的排Z、R、W | |
| D. | RY3、W2X、ZW5分子中每个原子最外层都达到8 电子结构 |