题目内容
通常情况下,CO与O2的混合气体m L,用电火花引燃后体积变为n L (在相同条件下测定)。(1)试确定原混合气体中CO的体积V(CO)。
(2)若反应后的气体密度在相同条件下为H2的15倍,试确定混合气体中各组分的物质的量之比。
解:(1)2CO + O2![]() 2CO2 ΔV
2CO2 ΔV
2 1 2 1
2(m-n) L (m-n) L (m-n) L
若O2过量,则V(CO)=2(m-n) L;
若CO过量,则V(CO)=[m-(m-n)] L=n L.
(2)因为![]() r(混)=2×15=30
r(混)=2×15=30
所以由平均值规律知,反应后的混合气体为CO和CO2.
所以由十字交叉法:
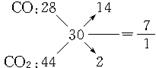
得:n(CO):n(CO2)=7:1.

练习册系列答案
相关题目