题目内容
通常情况下,CO与O2的混合气体(1)试确定原混合气体中CO与O2的体积。?
(2)若反应后的气体密度在相同条件下为氢气的15倍时,试确定反应气体的组成及物质的量之比。?????
解析:由反应:2CO + O2![]() 2CO2
2CO2 ![]() ??
??
2 1 2 1?
![]()
![]()
![]() ??
??
可知:A.当两者恰好完全作用时,V(CO)= 2![]() L V(O2)=
L V(O2)= ![]() L??
L??
B.当CO过量时,过量的CO的体积![]() L?
L?
原混合物中V(O2)=![]() L V(CO)=
L V(CO)=![]() L?
L?
C.当O2过量时,过量的O2的体积=![]() L?
L?
原混合物中V(CO)=2![]() 升 V(O2)=
升 V(O2)=![]() L?
L?
若反应后的气体密度在相同条件下为氢气的15倍时,混合气体的平均分子量是30,由于产物中肯定有CO2,它的相对分子质量大于30,所以另一种气体的相对分子质量必小于30,另一种气体只能是CO(也就是说O2不可能有余),该混合气体的组成可用下法求得:?
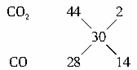 ?
?
可得:V(CO2)∶V (CO)=1∶7?
答案:(1)A.当两者恰好完全作用时,V(CO)=2![]() L ?V(O2)=
L ?V(O2)=![]() L??
L??
B.当CO过量时,过量的CO的体积![]() L,原混合物中V(O2 )=
L,原混合物中V(O2 )=![]() L?V(CO)=
L?V(CO)=![]() L;?
L;?
C.当O2过量时,过量的O2的体积
![]() L;原混合物中V(CO)=2
L;原混合物中V(CO)=2![]() L,V(O2)=
L,V(O2)=![]() L;?
L;?
(2)CO2与CO的体积比为1∶7。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目