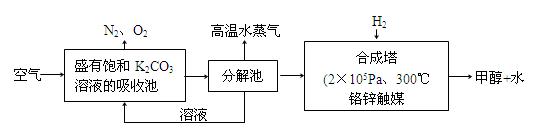
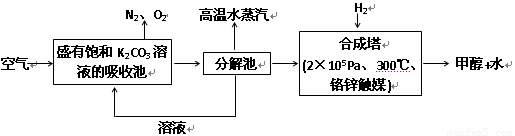
��Ŀ����
ͨ������£���������CO2�������������0.050%ʱ�����������Ե�����ЧӦ��Ϊ��С������CO2�Ի�����Ӱ�죬������������CO2��������ͬʱҲ��ǿ��CO2�������õ��о���
(1)Ŀǰ���ƹ��ó��ٽ�CO2��������̬��Һ̬֮�䣩��������������������һ�����Ի����Ļ��������� ��
(2)��ѧ��Ϊ��ȡ�����е�CO2���ѿ�������̼�����Һ��Ȼ���ٰ�CO2����Һ����ȡ����������ѧ��Ӧʹ֮��Ϊ������ȼ�ϼ״���������ͼ��
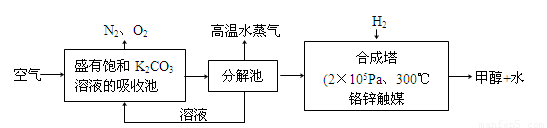
�ٷֽ���з�Ӧ�Ļ�ѧ����ʽΪ�� ��
�ںϳ����У�����4.4g CO2������H2ǡ�÷�Ӧ������̬����ų�4.947kJ��������д���÷�Ӧ���Ȼ�ѧ����ʽ�� ��
(3)ijͬѧ���ó������ⶨ������CO2����������������CaCO3��BaCO3���ܶȻ�Ksp�ֱ�Ϊ4.96��10-9��2.58��10-9������ý�����ͨ�������� ��Һ��ʵ��ʱ���ⶨ�¶ȡ�ѹǿ�Ϳ���������⣬����ⶨ ��
(1)���������㣨3�֣�
��2����2KHCO3 K2CO3+CO2��+H2O ��3�֣�
��CO2(g)+3H2(g) CH3OH(g)+H2O(g)
��H=-49.47kJ/mol ��3�֣�
��3��Ba(OH)2(��NaOH��BaCl2�����Һ)��3�֣� ���ɳ�����������3�֣�
����������