题目内容
两个极易导热的密闭容器A和B,容器A的容积恒定,容器B容积可变,在温度、压强和起始体积相同的条件下,向A和B中分别充入等物质的量的NO2,发生反应2NO2![]() N2O4(g)+Q.则:
N2O4(g)+Q.则:
(1)反应起始时,两容器中的反应速率大小关系________.
(2)两容器内的反应达到平衡时,压强间关系________.
(3)反应达到平衡时,两容器内NO2的浓度关系________.
答案:
解析:
解析:
|
(1)相等 (2)B中的压强比A中的大 (3)B中的NO2的浓度大于A中的NO2浓度 导解:起始时,NO2浓度相同,所以反应速率相等;该正反应为一个体积缩小的反应,随着反应的进行,气体的物质的量在减小,A中容积不变,所以压强减小;因为A,B中反应达到平衡时,温度相同,所以平衡常数相同,K= |

练习册系列答案
相关题目
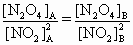 ,B中NO2转化率大,[N2O4]B>[N2O4]A,所以[NO2]A<[NO2]B.
,B中NO2转化率大,[N2O4]B>[N2O4]A,所以[NO2]A<[NO2]B. 两个极易导热的材料做成的体积相等的容器A和B,A是密闭定容的,B带上下可移动的活塞(气体不渗漏).在等温下向A、B两容器中充入等物质的量的N2O4固体并使之迅速气化.
两个极易导热的材料做成的体积相等的容器A和B,A是密闭定容的,B带上下可移动的活塞(气体不渗漏).在等温下向A、B两容器中充入等物质的量的N2O4固体并使之迅速气化. 2NO2的反应是气体体积增大的反应,A容器定容,B容器定压,随着反应的进行PA>PB,所以vA>vB
2NO2的反应是气体体积增大的反应,A容器定容,B容器定压,随着反应的进行PA>PB,所以vA>vB

 N2O4(g),以下正确的是:
N2O4(g),以下正确的是: