题目内容
(1)常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5 mol?L-1.若忽略水的电离及H2CO3的第二级电离.则H2CO3?HCO3-+H+的平衡常数K1=
(2)已知常温下Ksp(BaCO3)=5.1×10-9,Ksp(BaSO4)=1.1×10-10.
①把BaCO3和BaSO4的混合物投入水中,搅拌,制成悬浊液,再静止.上层清液中c(CO32-)与c(SO42-)之比是
②在BaSO4的悬浊液加入Na2CO3溶液,可使BaSO4转化为BaCO3.要生成BaCO3,Na2CO3溶液的浓度应大于
≈1)
4.2×10-7
4.2×10-7
.(已知10-5.60=2.5×10-6)(2)已知常温下Ksp(BaCO3)=5.1×10-9,Ksp(BaSO4)=1.1×10-10.
①把BaCO3和BaSO4的混合物投入水中,搅拌,制成悬浊液,再静止.上层清液中c(CO32-)与c(SO42-)之比是
46:1
46:1
.②在BaSO4的悬浊液加入Na2CO3溶液,可使BaSO4转化为BaCO3.要生成BaCO3,Na2CO3溶液的浓度应大于
5.1×10-4
5.1×10-4
mol/L.(设定:| 1.1 |
分析:(1)平衡常数K1=
;
(2)①c(CO32-):c(SO42-)=
:
=Ksp(BaCO3):Ksp(BaSO4);
②根据Ksp(BaSO4)计算BaSO4的悬浊液中c(Ba2+),再根据Ksp(BaCO3)计算使Ba2+沉淀需要c(CO32-),据此计算碳酸钠的浓度.5.1×10-4
| C(HCO3-).C(H+) |
| C(H2CO3) |
(2)①c(CO32-):c(SO42-)=
| Ksp(BaCO3) |
| C(Ba2+) |
| Ksp(BaSO4) |
| C(Ba2+) |
②根据Ksp(BaSO4)计算BaSO4的悬浊液中c(Ba2+),再根据Ksp(BaCO3)计算使Ba2+沉淀需要c(CO32-),据此计算碳酸钠的浓度.5.1×10-4
解答:解:(1)忽略水的电离及H2CO3的第二级电离,溶液的pH=5.60的碳酸,故c(H+)=c(HCO3-)=1×10-5.6 mol?L-1,溶液中c(H2CO3)=1.5×10-5 mol?L-1,故平衡常数K1=
=
=4.2×10-7,
故答案为:4.2×10-7;
(2)①c(CO32-):c(SO42-)=
:
=Ksp(BaCO3):Ksp(BaSO4)=5.1×10-9:1.1×10-10
=46:1,
故答案为:46:1;
②BaSO4的悬浊液中c(Ba2+)=c(SO42-)=
mol/L=1×10-5mol/L,故使Ba2+沉淀需要碳酸根的最小浓度为c(CO32-)=
=
mol/L=5.1×10-4mol/L,
故答案为:5.1×10-4mol/L.
| C(HCO3-).C(H+) |
| C(H2CO3) |
| 1×10-5.6×1×10-5.6 |
| 1.5×10-5 |
故答案为:4.2×10-7;
(2)①c(CO32-):c(SO42-)=
| Ksp(BaCO3) |
| C(Ba2+) |
| Ksp(BaSO4) |
| C(Ba2+) |
=46:1,
故答案为:46:1;
②BaSO4的悬浊液中c(Ba2+)=c(SO42-)=
| 1.1×10-10 |
| Ksp(BaCO3) |
| c(Ba2+) |
| 5.1×10-9 |
| 1×10-5 |
故答案为:5.1×10-4mol/L.
点评:本题考查了难溶电解质的溶解平衡、弱电解质的电离等知识点,难点是根据溶度积常数计算离子浓度,根据公式来分析解答即可.

练习册系列答案
相关题目
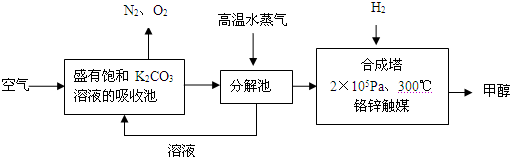
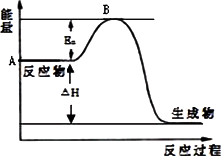
 的ΔH为____________________。
的ΔH为____________________。 的ΔH为____________________。
的ΔH为____________________。