题目内容
(2011?广东)下列实验现象预测正确的是( )


分析:A.溴和NaOH反应,苯不溶于水,且密度比水小;
B.浓硫酸和蔗糖反应生成二氧化碳和二氧化硫气体;
C.生成NO,根据NO的性质判断;
D.在沸水中滴加饱和氯化铁溶液可生成氢氧化铁胶体.
B.浓硫酸和蔗糖反应生成二氧化碳和二氧化硫气体;
C.生成NO,根据NO的性质判断;
D.在沸水中滴加饱和氯化铁溶液可生成氢氧化铁胶体.
解答:解:A.溴和NaOH反应生成NaBr和NaBrO,苯不溶于水,且密度比水小,所以上层无色,故A错误;
B.浓硫酸和蔗糖反应生成二氧化碳和二氧化硫气体,二氧化硫与酸性高锰酸钾发生氧化还原反应,二氧化碳不反应,故B正确;
C.生成NO,NO易与空气中氧气反应生成二氧化氮,为红棕色,故C错误;
D.在沸水中滴加饱和氯化铁溶液可生成氢氧化铁胶体,当光束通过体系时可产生丁达尔效应,故D正确.
故选BD.
B.浓硫酸和蔗糖反应生成二氧化碳和二氧化硫气体,二氧化硫与酸性高锰酸钾发生氧化还原反应,二氧化碳不反应,故B正确;
C.生成NO,NO易与空气中氧气反应生成二氧化氮,为红棕色,故C错误;
D.在沸水中滴加饱和氯化铁溶液可生成氢氧化铁胶体,当光束通过体系时可产生丁达尔效应,故D正确.
故选BD.
点评:本题考查化学实验基本操作,题目难度中等,解答本题的关键是把握相关物质的性质,学习中注意积累.

练习册系列答案
相关题目
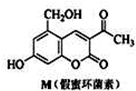 (2011?广东模拟)化合物M叫假蜜环菌甲素,它是香豆素类天然化合物.对M的性质叙述正确的是( )
(2011?广东模拟)化合物M叫假蜜环菌甲素,它是香豆素类天然化合物.对M的性质叙述正确的是( )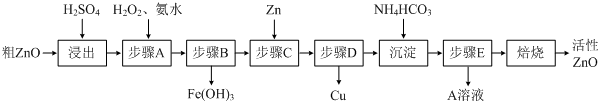
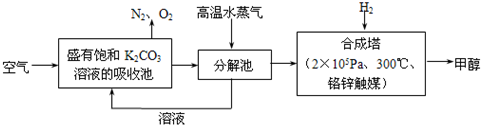



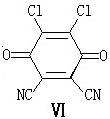 )分子获得2个氢原子后,转变成1个芳香族化合物分子,该芳香族化合物分子的结构简式为
)分子获得2个氢原子后,转变成1个芳香族化合物分子,该芳香族化合物分子的结构简式为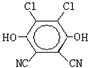
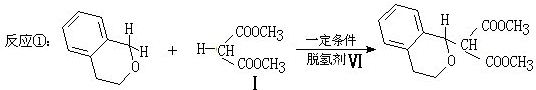
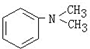 与1分子
与1分子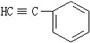 在一定条件下可发生类似①的反应,其产物分子的结构简式为
在一定条件下可发生类似①的反应,其产物分子的结构简式为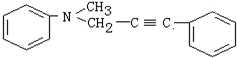
 (2011?广东)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2.紫外光照射时,在不同催化剂(I,II,III)作用下,CH4产量随光照时间的变化如图所示.
(2011?广东)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2.紫外光照射时,在不同催化剂(I,II,III)作用下,CH4产量随光照时间的变化如图所示.