题目内容
【题目】工业上常用还原沉淀法处理含铬废水(![]() 和
和![]() ),其流程为:
),其流程为:
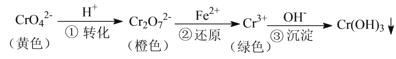
已知:步骤③生成的![]() 在溶液中存在以下沉淀溶解平衡:
在溶液中存在以下沉淀溶解平衡:![]()
![]() ,
,![]()
下列有关说法不正确的是
A.步骤①中当![]() 时,说明反应:
时,说明反应:![]() 达到平衡状态
达到平衡状态
B.若向![]() 溶液中加NaOH浓溶液,溶液可由橙色变黄色
溶液中加NaOH浓溶液,溶液可由橙色变黄色
C.步骤②中,若要还原![]() 离子,需要
离子,需要![]()
D.步骤③中,当将溶液的pH调节至5时,可认为废水中的铬元素已基本除尽![]() 当溶液中
当溶液中![]() 时,可视作该离子沉淀完全
时,可视作该离子沉淀完全![]()
【答案】C
【解析】
该还原沉淀法处理含铬(![]() 和
和![]() )废水的过程是:先加酸使
)废水的过程是:先加酸使![]() 转化成
转化成![]() ,该步是含同价态Cr的不同离子之间的转化;随后,用亚铁盐将
,该步是含同价态Cr的不同离子之间的转化;随后,用亚铁盐将![]() 还原为Cr3+,该步发生的是氧化还原反应;最后调节pH,使Cr3+形成Cr(OH)3沉淀。结合化学平衡、氧化还原反应、溶度积等知识可解各小题。
还原为Cr3+,该步发生的是氧化还原反应;最后调节pH,使Cr3+形成Cr(OH)3沉淀。结合化学平衡、氧化还原反应、溶度积等知识可解各小题。
A. 步骤①中当![]() 时,说明正逆反应速率相等,各组分浓度不再变化,则反应
时,说明正逆反应速率相等,各组分浓度不再变化,则反应![]() 达到平衡状态,故A正确;
达到平衡状态,故A正确;
B. 过程![]() (黄色)
(黄色)![]()
![]() (橙色)的反应为:
(橙色)的反应为:![]() ,则加NaOH浓溶液,平衡逆向移动,
,则加NaOH浓溶液,平衡逆向移动,![]() 会转化成
会转化成![]() ,溶液可由橙色变黄色,故B正确;
,溶液可由橙色变黄色,故B正确;
C. 还原![]() 离子,转移电子为
离子,转移电子为![]() ,Fe元素的化合价由+2升高为+3,则由电子守恒可知,需要
,Fe元素的化合价由+2升高为+3,则由电子守恒可知,需要![]() ,故C错误;
,故C错误;
D. 步骤③中,当将溶液的pH调节至5时,c(OH-)=10-9mol/L,由Ksp可知,![]() ,则可认为废水中的铬元素已经除尽,故D正确;
,则可认为废水中的铬元素已经除尽,故D正确;
答案选C。

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目