题目内容
草酸(H2C2O4)是二元弱酸,草酸氢钾溶液呈酸性。在0.1mol·L-1 KHC2O4溶液中,下列关系正确的是
A、c(K+)+c(H+) = c(HC2O4-)+c(OH-)+c(C2O42-)
B、c(HC2O4-)+c(C2O42-) = 0.1 mol·L-1
C、c(C2O42-) < c(H2C2O4)
D、c(K+) = c(H2C2O4)+c(HC2O4-)+c(C2O42-)
【答案】
D
【解析】
试题分析:A、在溶液中存在电荷守恒:c(K+)+c(H+)=c(HC2O4-)+c(OH-)+2c(C2O42-),故A错误;B、溶液中总存在物料守恒:c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.1mol/L,故B错误;C、KHC2O4溶液呈酸性,说明HC2O4-的电离程度大与水解程度,即c(C2O42-)>c(H2C2O4),故C错误。D、由电荷守恒和物料守恒,联立可得到:(K+)=c(H2C2O4)+c(HC2O4-)+c(C2O42-),故D正确。
考点:盐类水解的应用;离子浓度大小的比较

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案
相关题目



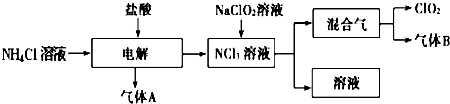
 用二氧化氯(ClO2)、高铁酸钠(Na2FeO4摩尔质量为166g?mol-1)等新型净水剂替代传统的净水剂Cl2对淡水进行消毒是城市饮用水处理新技术.ClO2和Na2FeO4在水处理过程中分别被还原为Cl-和Fe3+.
用二氧化氯(ClO2)、高铁酸钠(Na2FeO4摩尔质量为166g?mol-1)等新型净水剂替代传统的净水剂Cl2对淡水进行消毒是城市饮用水处理新技术.ClO2和Na2FeO4在水处理过程中分别被还原为Cl-和Fe3+.