��Ŀ����
�±�ΪԪ�����ڱ���һ���֣�����Ԫ�آ١����ڱ��е�λ�ã����û�ѧ����ش��������⣺
��1���ܡ��ݡ��ߵ�ԭ�Ӱ뾶�ɴ�С��˳��Ϊ (��Ԫ�ط��ű�ʾ����ͬ)��
��2���͢ߵ���ۺ����������ǿ��Ϊ > ��
��3���١�������Ԫ�ذ�ԭ�Ӹ���֮��Ϊ1��1��ɵij���Һ̬�������������Һ���ܽ�Fe2��������д���÷�Ӧ�����ӷ���ʽ ��
��4���ɱ���Ԫ���γɵ����ʿɷ�����ͼ�еķ�Ӧ������B��C��G�ǵ��ʣ�BΪ����ɫ���壬D��Һ�Լ��ԡ�
��д��D��Һ��G��Ӧ�Ļ�ѧ����ʽ ��
��д������A��Һ�����ʵ������ӵķ����� ��
�۳����£������1 L 0.1 mol/L��A��Һ��һ��ʱ�������ҺpHΪ12(������Һ����仯)����õ�������ת�Ƶ��ӵ����ʵ���Ϊ mol��
������ͼ�и�����Ӧ��Ϊǡ����ȫת����������X�к��е������� ��
��15�֣�ÿ��2�֣�
��1��Na��Cl��F ��2��HClO4 H2SO4
��3��H2O2��2Fe2����2H��==2Fe3����2H2O
��4����2Al��2NaOH��2H2O==2NaAlO2��3H2��
��ȡ����A��Һ�μӼ���(ϡ�����ữ��)��������Һ�а�ɫ��������
��0.01 ��Al(OH)3��H2O��NaCl��3�֣�
�����������������Ԫ���������ڱ��е�λ�ã���֪Ԫ�ص����࣬��ΪHԪ�أ���ΪOԪ�أ���ΪAlԪ�أ���ΪFԪ�أ���ΪNaԪ�أ���ΪSԪ�أ���ΪClԪ�أ�
�ŵ��Ӳ�Խ��뾶Խ������Na��Cl��F�����Ӳ�һ�����ԭ�ӣ��˵����Խ��뾶ԽС����Na��Cl���ʴ�Ϊ��Na��Cl��F�ܡ��ݡ��ߵ�ԭ�Ӱ뾶�ɴ�С��˳��ΪNa��Cl��F���𰸣�Na��Cl��F���Ƣ�ΪSԪ�أ���ΪClԪ�أ���ͬһ����Ԫ�ص�ԭ�ӣ�����Ԫ�������ɣ�����������������Ӧˮ�������������ǿ���������ԣ�HClO4 H2SO4���𰸣�HClO4 H2SO4���Ǣ�ΪHԪ�أ���ΪOԪ�أ��١�������Ԫ�ذ�ԭ�Ӹ���֮��Ϊ1��1��ɵij���Һ̬��������H2O2��H2O2���������ԣ��ܽ�Fe2�� ������Fe3�� ������ʽΪ��H2O2��2Fe2����2H��==2Fe3����2H2O���𰸣�H2O2��2Fe2����2H��==2Fe3����2H2O��
���㣺Ԫ�������ɺ�Ԫ�����ڱ����ۺ�Ӧ��

��X��Y��Z��W���ֺ�14�����ӵ����ӣ���ṹ�ص����£�
| ���Ӵ��� | X | Y | Z | W |
| ԭ�Ӻ��� | ���� | ��ͬԪ�ع��ɵ����� | ͬԪ�ع��ɵ����� | ͬԪ�ع��ɵ����� |
| ���ӵĵ���� | 0 | 0 | ��������� | 0 |
(1)Aԭ�Ӻ����Xԭ�Ӷ�3�����ӣ�A��ԭ�ӽṹʾ��ͼ�� ����lmolX�������ᄃ���к��й��ۼ���ĿΪ ��
(2)Z���������ɵĻ�����ĵ���ʽΪ ��
(3)14gY��ȫȼ�շų���������141.5kJ��д��Yȼ�յ��Ȼ�ѧ����ʽ ��
(4)���W��Ԫ������������Ӧ��ˮ���������ͼ��ʾת����ϵ����Ϊ�������ʣ���Ӧ�����������������ԣ�

��д����Ԫ�������ڱ��е�λ�� ��
��д�����ڸ�������ˮ��Ӧ�Ļ�ѧ����ʽ ��
�����W��Ԫ�صļ��⻯�K������ˮ����Ҫԭ���� �����⻯����������Թ���һ��ȼ�ϵ�أ��������Һ��KOH���为���ĵ缫��ӦʽΪ ��
�±�������Ԫ�����ڱ����ֶ����ڵ�����Ԫ��
| | W | X | Y | |
| R | | | | Z |
��֪RΪ�ؿ��к������Ľ���Ԫ�ء�
��1��д��Z��ԭ�ӽṹʾ��ͼ________��
��2��W����ԭ���γ�6ԭ�ӷ��ӵĽṹ��ʽ_______��
��3����ϸRX��ĩ��Ӧ���ڴ��ģ���ɵ�·����������ԭ��ΪR2Y3��X2��W�ڸ����·�Ӧ�������ֻ���������ֻ������������Ԫ����ɣ���ԭ�Ӹ����Ⱦ�Ϊ1��1���䷴Ӧ�Ļ�ѧ����ʽΪ_______��
��4��X����������Ӧˮ������X��̬�⻯�ﷴӦ������������ˮ�У�������Һ����Ũ�ȴӴ�С��˳����_______��
��5�������������ȼ����(N2H4)��������N2O4��Ӧ����N2��ˮ������
��֪��N2(g)+2O2(g)=N2O4(l) ��H1=��195kJ?mol��1
��N2H4(l) +O2(g)=N2(g)+2H2O(g) ��H2=��534.2kJ?mol��1
д���º�N2O4��Ӧ���Ȼ�ѧ����ʽ______________��
��6���¶�ΪTʱ����2.0L�����ܱ������г���1.00 mol PCl5����ӦPCl5(g)
 PCl3(g)+Cl2(g)������һ��ʱ�䣨t)��ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���
PCl3(g)+Cl2(g)������һ��ʱ�䣨t)��ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±���| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
��ͬ�¶��£���ʼʱ�������г���1.00 mol PC15��0.20 mol PCl3��0.40 mol Cl2����Ӧ�ﵽƽ��ǰv(��) _______v(�棩���>����=����<������ԭ����_______��
X��Y��Z��W��Ԫ�����ڱ�ǰ�������еij���Ԫ�أ��������Ϣ���±���
| Ԫ�� | �����Ϣ |
| X | Xԭ�ӵ�L���������K���������2�� |
| Y | Yԭ�ӵ����������Ų�ʽΪ��nsnnpn+2 |
| Z | Z����������Ϊ23��������Ϊ12��ԭ�Ӻ� |
| W | W�ж��ֻ��ϼۣ����ɫ���������ڿ����л�Ѹ�ٱ�ɻ���ɫ������ɺ��ɫ |
��2��X�Ļ����Ա�Y�� (�ǿ��������)��X��Y����̬�⻯���У����ȶ����� (д��ѧʽ)��
��3��д��Z2Y2�ĵ���ʽ ��XY2�Ľṹʽ ��
��4����Xԭ������ԭ���γɵĶ��ַ����У���Щ���ӵĺ˴Ź���������ʾ�������⣬д������һ�ַ��ӵ����� ����Ԫ�ء�X��Y��ԭ��Ҳ�ɹ�ͬ�γɶ��ַ��Ӻ�ij�ֳ����������ӣ�д������һ�ַ�������������ӷ�Ӧ�����ӷ���ʽ ��

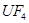 +
+ 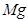 ����
����  +
+ 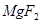
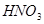 ����
���� 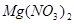 +
+ 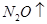 +
+