题目内容
将0.3mol NaCl固体与0.1mol CuSO4?5H2O固体混合溶于水,配成1升混合液.然后取出200ml溶液,用石墨电极,通电一段时间(不考虑水解).
求Cl-正好全部变为氯气逸出时,阴极上产生的气体体积(标准状况下)是多少?
所得溶液的pH为多少(假设溶液体积不变)?
求Cl-正好全部变为氯气逸出时,阴极上产生的气体体积(标准状况下)是多少?
所得溶液的pH为多少(假设溶液体积不变)?
分析:(1)根据溶液中阴阳离子的放电顺序,判断每一阶段放电的离子,然后写出电解反应的离子方程式;
(2)先确定最后阶段放电的离子,再写出阴极上发生的电极反应式;
(3)先根据题意判断当阴极有气体产生时发生的电解反应,然后计算铜全部析出时剩余的氯离子的物质的量,根据氯离子的物质的量计算阴极上生成气体的体积.
(2)先确定最后阶段放电的离子,再写出阴极上发生的电极反应式;
(3)先根据题意判断当阴极有气体产生时发生的电解反应,然后计算铜全部析出时剩余的氯离子的物质的量,根据氯离子的物质的量计算阴极上生成气体的体积.
解答:解:根据题意知,取出的溶液中含有的溶质的物质的量分别为:NaCl 0.06mol,CuSO4 0.02mol;溶液中阴阳离子的放电顺序分别为:阳离子放电顺序Cu2+>H+>Na+,阴离子放电顺序为Cl->OH->SO42-,所以,该溶液电解三个阶段分别为:
第一阶段:Cu2+和Cl-放电,生成氯气和铜.阴极电极反应Cu2++2e-=Cu,阳极电极反应2Cl--2e-=Cl2↑;
根据得失电子相等知,铜离子先完全电解,氯离子还剩0.02mol,所以发生第二阶段电解反应;
第二阶段:H+ 和Cl-放电,生成氢气和氯气;
根据得失电子相等知,氯离子完全电解,发生第三阶段反应,
第三阶段:H+ 和OH-放电,生成氢气和氧气.
根据以上分析知,第一阶段的电解反应为Cu2++2Cl-
Cu+Cl2
电解的最后阶段,H+ 在阴极上放电,OH-的阳极上放电,分别生成氢气和氧气.
第一阶段根据得失电子相等知,铜离子先完全电解,氯离子还剩0.02mol,所以发生第二阶段电解反应;
当阴极上有气体生成时,发生的电解反应为:
2Cl-+2H2O
Cl2↑+H2↑+2OH-
2 22.4L 2
0.02mol 0.224L 0.02mol
阴极上生成氢气0.224L;生成氢氧根离子浓度=
=0.1mol/L
溶液pH=13.
答:Cl-正好全部变为氯气逸出时,阴极上产生的气体体积(标准状况下)是 0.224L;所得溶液的pH为13.
第一阶段:Cu2+和Cl-放电,生成氯气和铜.阴极电极反应Cu2++2e-=Cu,阳极电极反应2Cl--2e-=Cl2↑;
根据得失电子相等知,铜离子先完全电解,氯离子还剩0.02mol,所以发生第二阶段电解反应;
第二阶段:H+ 和Cl-放电,生成氢气和氯气;
根据得失电子相等知,氯离子完全电解,发生第三阶段反应,
第三阶段:H+ 和OH-放电,生成氢气和氧气.
根据以上分析知,第一阶段的电解反应为Cu2++2Cl-
| ||
电解的最后阶段,H+ 在阴极上放电,OH-的阳极上放电,分别生成氢气和氧气.
第一阶段根据得失电子相等知,铜离子先完全电解,氯离子还剩0.02mol,所以发生第二阶段电解反应;
当阴极上有气体生成时,发生的电解反应为:
2Cl-+2H2O
| ||
2 22.4L 2
0.02mol 0.224L 0.02mol
阴极上生成氢气0.224L;生成氢氧根离子浓度=
| 0.02mol |
| 0.2L |
溶液pH=13.
答:Cl-正好全部变为氯气逸出时,阴极上产生的气体体积(标准状况下)是 0.224L;所得溶液的pH为13.
点评:本题考查了电解原理的分析判断,解题时注意以下几点:混合溶液中离子的放电顺序.发生电解反应的三个阶段.只有明确知道这些问题才能正确解答本题,题目难度较大.

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目

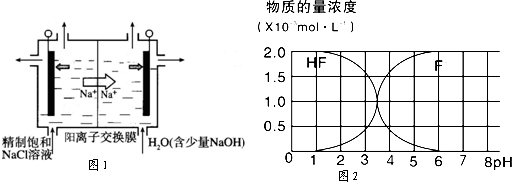
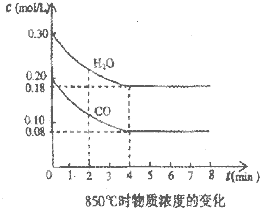 Ⅰ、(1)在25℃条件下将pH=3的醋酸稀释100倍后溶液的pH为
Ⅰ、(1)在25℃条件下将pH=3的醋酸稀释100倍后溶液的pH为