题目内容
2a L Fe2(SO4)3和(NH4)2SO4的混合溶液分成两等份,向其中一份加入b mol的BaCl2溶液,恰好使溶中的SO42-完全沉淀;向另外一等份加入足量NaOH固体并加热可得到c mol NH3,则原溶液中Fe3+的物质的量浓度为( )mol·L-1
A. | B. | C. | D. |
C
解析试题分析:把混合溶液等分为两份,由混合溶液中加入bmolBaCl2,恰好使溶液中的SO42-离子完全沉淀,则SO42-+Ba2+═BaSO4↓,c(SO42-)="b/a" mol/L, 在另一份加入足量氢氧化钠,
则NH4++OH-△NH3↑+H2Oc(NH4+)="c/a" mol/L,又溶液不显电性,设原溶液中的Fe3+浓度为x,由电荷守恒可知,x×3+a/c mol/L×1=b/a mol/L×2,解得x= ,故选C
,故选C
考点:物质的量浓度相关计算
点评:本题考查物质的量浓度的计算,明确发生的离子反应及溶液不显电性是解答本题的关键,并熟悉浓度的计算公式来解答即可.

练习册系列答案
相关题目


 C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是________
C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是________ 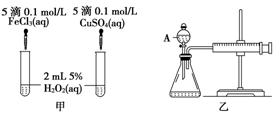
 C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是________
C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是________