题目内容
8.某一元弱酸(用HA表示)在水中的电离方程式是:HA?H++A-,回答下列问题:(1)向溶液中加入适量NaA固体,以上平衡将向逆(填“正”、“逆”)反应方向移动.
(2)若向溶液中加入适量NaCl溶液,以上平衡将向正向(填“正向”、“逆向”、或“不移动”)移动,溶液pH将增大中(填“增大”、“减小”或“不变”),溶液中$\frac{c({A}^{-})}{c(HA)•c(O{H}^{-})}$比值不变(填“增大”、“减小”或“不变”).
(3)在25℃下,将a mol•L-1的氨水与0.01mol•L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液呈中性,用含a的代数式表示NH3•H2O的电离常数Kb=$\frac{1{0}^{-9}}{a-0.01}$.
分析 (1)向溶液中加入适量NaA固体,c(A-)增大,结合浓度对平衡移动的影响分析;
(2)加水稀释促进弱电解质的电离,溶液体积增大,c(A-)和c(H+)减小,Kw、Ka不变;
(3)在25℃下,平衡时溶液中c(NH4+)=c(Cl-)=0.005mol/L,根据物料守恒得c(NH3.H2O)=(0.5a-0.005)mol/L,根据电荷守恒得c(H+)=c(OH-)=10-7mol/L,溶液呈中性,NH3•H2O的电离常数Kb=$\frac{c(O{H}^{-}).c(N{{H}_{4}}^{-})}{c(N{H}_{3}.{H}_{2}O)}$.
解答 解:(1)向溶液中加入适量NaA固体,c(A-)增大,平衡向逆方向移动;
故答案为:逆;
(2)若向溶液中加入适量NaCl溶液,NaCl与HA不反应,相当于加水,加水稀释促进弱电解质的电离,平衡向正方向移动,溶液体积增大,c(A-)和c(H+)减小,则pH增大,$\frac{c({A}^{-})}{c(HA)•c(O{H}^{-})}$=$\frac{Ka}{Kw}$,Kw、Ka只受温度影响,所以$\frac{c({A}^{-})}{c(HA)•c(O{H}^{-})}$不变;
故答案为:正向;增大;不变;
(3)在25℃下,平衡时溶液中c(NH4+)=c(Cl-)=0.005mol/L,根据物料守恒得c(NH3.H2O)=(0.5a-0.005)mol/L,根据电荷守恒得c(H+)=c(OH-)=10-7mol/L,溶液呈中性,NH3•H2O的电离常数Kb=$\frac{c(O{H}^{-}).c(N{{H}_{4}}^{-})}{c(N{H}_{3}.{H}_{2}O)}$=$\frac{1{0}^{-7}×5×1{0}^{-3}}{0.5a-5×1{0}^{-3}}$=$\frac{1{0}^{-9}}{a-0.01}$;
故答案为:$\frac{1{0}^{-9}}{a-0.01}$.
点评 本题考查弱电解质的电离,题目难度中等,注意影响平衡移动的因素,易错点为电离常数的计算,注意把握计算公式的运用,侧重于考查学生的分析能力和计算能力.

 名校课堂系列答案
名校课堂系列答案| A. | 加热蒸干Na2CO3溶液,最后可以得到NaOH和Na2CO3的混合固体 | |
| B. | 除去MgCl2中的Fe3+,可以加入NaOH固体 | |
| C. | 明矾净水的反应:Al3++3H2O?Al(OH)3(胶体)+3H+ | |
| D. | 加热蒸干KCl溶液,最后得到KOH固体(不考虑CO2的反应) |
| A. | SO2、SiO2、CO2均为酸性氧化物 | |
| B. | 稀豆浆、硅酸、氯化铁溶液均为胶体 | |
| C. | 烧碱、冰醋酸、四氯化碳、氨气均为电解质 | |
| D. | 福尔马林、水玻璃、氢氟酸、小苏打均为纯净物 |
| A. | N2O3 | B. | NO2 | C. | N2O | D. | N2O4 |
| A. | 用O3替代Cl2作饮用水消毒剂更符合绿色化学的要求 | |
| B. | “光化学烟雾”、“臭氧空洞”的形成都与氮氧化合物有关 | |
| C. | 尽量使用含12C的产品,减少使用含13C或14C的产品符合“促进低碳经济”宗旨 | |
| D. | 高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强碱会“断路” |
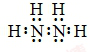 .
.
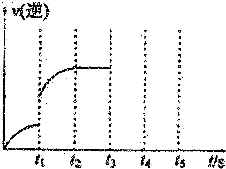 Ⅰ.体积为5L的恒温、恒容密闭容器甲起始投入2molN2、3molH2经过l0s达平衡,测得平衡时NH3的物质的量为0.8mol.
Ⅰ.体积为5L的恒温、恒容密闭容器甲起始投入2molN2、3molH2经过l0s达平衡,测得平衡时NH3的物质的量为0.8mol.