题目内容
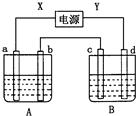
如图所示装置,X、Y为电源的两极,a、b均为石墨电极,c为铜电极,d为铁电极,A槽中盛装稀硫酸,B槽中盛装CuSO4溶液.通电一段时间后,发现d电极上覆盖一层红色物质.根据以上实验事实,回答下列问题:
(1)c极的电极反应式为______;
(2)A槽中发生反应的化学方程式为______ O2↑+H2↑

【答案】分析:通电一段时间后,发现d电极上覆盖一层红色物质,则d电极是电解池阴极,a、c电极是阳极,b是阴极,X是正极,Y是负极.
(1)c电极上失电子发生氧化反应;
(2)A槽中,阳极上氢氧根离子失电子发生氧化反应,阴极上氢离子得电子发生还原反应;
(3)根据A槽中酸浓度的变化判断pH的变化;
(4)根据B槽中氢离子浓度是否变化判断溶液的pH是否变化.
解答:解:通电一段时间后,发现d电极上覆盖一层红色物质,则d电极是电解池阴极,a、c电极是阳极,b是阴极,X是正极,Y是负极.
(1)c电极是电解池阳极,阳极上铜失电子发生氧化反应,电极反应式为:Cu-2e-=Cu2+,
故答案为:Cu-2e-=Cu2+;
(2)A槽中,阳极上氢氧根离子失电子发生氧化反应,阴极上氢离子得电子发生还原反应,实际上就是电解水,所以其电池反应式为:2H2O O2↑+H2↑,
O2↑+H2↑,
故答案为:2H2O O2↑+H2↑;
O2↑+H2↑;
(3)电解时,阳极上氢氧根离子失电子发生氧化反应,阴极上氢离子得电子发生还原反应,实际上就是电解水,溶质的物质的量不变,但溶剂的量减少,所以硫酸的物质的量浓度增大,溶液的pH减小,故答案为为:变小;
(4 )电解时,阳极上铜失电子进入溶液,阴极上铜离子得电子生成铜,溶液中硫酸铜的物质的量浓度不变,则溶液的pH不变,故答案为:不变.
点评:本题考查了电解原理,难度不大,注意电解含氧强酸和强碱实际上就是电解水,会导致溶液的物质的量浓度增大,从而引起溶液pH的变化.
(1)c电极上失电子发生氧化反应;
(2)A槽中,阳极上氢氧根离子失电子发生氧化反应,阴极上氢离子得电子发生还原反应;
(3)根据A槽中酸浓度的变化判断pH的变化;
(4)根据B槽中氢离子浓度是否变化判断溶液的pH是否变化.
解答:解:通电一段时间后,发现d电极上覆盖一层红色物质,则d电极是电解池阴极,a、c电极是阳极,b是阴极,X是正极,Y是负极.
(1)c电极是电解池阳极,阳极上铜失电子发生氧化反应,电极反应式为:Cu-2e-=Cu2+,
故答案为:Cu-2e-=Cu2+;
(2)A槽中,阳极上氢氧根离子失电子发生氧化反应,阴极上氢离子得电子发生还原反应,实际上就是电解水,所以其电池反应式为:2H2O
 O2↑+H2↑,
O2↑+H2↑,故答案为:2H2O
 O2↑+H2↑;
O2↑+H2↑;(3)电解时,阳极上氢氧根离子失电子发生氧化反应,阴极上氢离子得电子发生还原反应,实际上就是电解水,溶质的物质的量不变,但溶剂的量减少,所以硫酸的物质的量浓度增大,溶液的pH减小,故答案为为:变小;
(4 )电解时,阳极上铜失电子进入溶液,阴极上铜离子得电子生成铜,溶液中硫酸铜的物质的量浓度不变,则溶液的pH不变,故答案为:不变.
点评:本题考查了电解原理,难度不大,注意电解含氧强酸和强碱实际上就是电解水,会导致溶液的物质的量浓度增大,从而引起溶液pH的变化.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
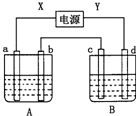 如图所示装置,X、Y为电源的两极,a、b均为石墨电极,c为铜电极,d为铁电极,A槽中盛装稀硫酸,B槽中盛装CuSO4溶液.通电一段时间后,发现d电极上覆盖一层红色物质.
如图所示装置,X、Y为电源的两极,a、b均为石墨电极,c为铜电极,d为铁电极,A槽中盛装稀硫酸,B槽中盛装CuSO4溶液.通电一段时间后,发现d电极上覆盖一层红色物质.